对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列研究结果和示意图相符的是( )
| A | B | C | D | |
| 研究 结果 | 压强对反应的影响 | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 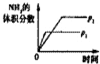 | 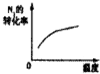 | 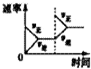 |  |
| A、A | B、B | C、C | D、D |
对于反应mA(g)+nB(g)?pC(g)+qD(g) 满足下列图象,根据图象判断四种关系正确的是( )

| A、m+n>p+q,正反应吸热 |
| B、m+n<p+q,正反应放热 |
| C、m+n>p+q,正反应放热 |
| D、m+n<p+q,正反应吸热 |
 可逆反应在一定条件下达到平衡后,速率差值[即v(正)-v(逆)]与压强的变化曲线如图所示,其中与曲线①相符的反应为( )
可逆反应在一定条件下达到平衡后,速率差值[即v(正)-v(逆)]与压强的变化曲线如图所示,其中与曲线①相符的反应为( )| A、2SO3(g)?2SO2(g)+02(g) |
| B、H2(g)+I2(g)?2HI(g) |
| C、C(s)+H2O(g)?C0(g)+H2(g) |
| D、N2(g)+3H2(g)?2NH3(g) |
一定量的液态化合物A在体积固定密闭容器中,在一定条件下与67.2mL X2(已转化为标准状况下)恰好完全反应A(液)+3X2(气)=B(气)+nC(气),冷却后在标准状况下,测得混合气体压强减小,则n值为( )
| A、1 | B、2 | C、3 | D、4 |
某兴趣小组为探究温度、压强对可逆反应A(g)+B(g)??C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的量浓度为[浓度1].然后改变外界条件又做了两组实验:①只升高温度;②只改变体系压强;分别测得新平衡时容器中各物质的量浓度为[浓度2]、[浓度3].
请找出实验操作①②与实验数据[浓度2]、[浓度3]的对应关系,并分析下列结论,其中错误的是( )
| A | B | C | |
| 浓度1 | 0.05mol?L-1 | a mol?L-1 | 0.05 mol?L-1 |
| 浓度2 | 0.078 mol?L-1 | 0.078 mol?L-1 | 0.122 mol?L-1 |
| 浓度3 | 0.06 mol?L-1 | 0.06 mol?L-1 | 0.04 mol?L-1 |
| 浓度4 | 0.07 mol?L-1 | 0.07 mol?L-1 | 0.098 mol?L-1 |
| A、由[浓度3]与[浓度1]的比较,可判断出正反应是放热反应 |
| B、由[浓度2]与[浓度1]的比较,可判断平衡移动的原因是升高温度 |
| C、[浓度1]中a=0.05 |
| D、该组某学生在实验①过程中,测得各物质在某一时刻的浓度为[浓度4].与[浓度1]比较,可发现该同学在测定[浓度4]这组数据时出现了很大的误差 |
 将物质的量均为2.0mol的物质X、Y混合,发生如下反应:2X(g)+Y(g)?2W(g).在反应过程中W的物质的量分数随温度变化如图所示,下列判断不正确的是( )
将物质的量均为2.0mol的物质X、Y混合,发生如下反应:2X(g)+Y(g)?2W(g).在反应过程中W的物质的量分数随温度变化如图所示,下列判断不正确的是( )| A、T0对应的V(正)和V(逆)的关系是:V(正)=V(逆) |
| B、此反应的正反应为放热反应 |
| C、A、B两点正反应速率的大小关系是:V(A)=V(B) |
| D、若B点的W的物质的量分数为50.0%,则参加反应的X的物质的量为1.6mol |
150℃、101kPa时,由两种烃组成的混合气体0.5L在4.5L O2中完全燃烧,测得反应后气体总体积小于5L,其中含CO2 0.8L,则生成水蒸汽的体积为( )
| A、0.7 L |
| B、1.4 L |
| C、1.6 L |
| D、2.8 L |
0.116g饱和一元醛,进行银镜反应时析出0.432g银.则该醛为( )
| A、丙醛 | B、乙醛 | C、甲醛 | D、苯酚 |
 根据如图填空.
根据如图填空.