题目内容
对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列研究结果和示意图相符的是( )
| A | B | C | D | |
| 研究 结果 | 压强对反应的影响 | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 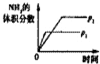 | 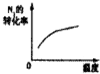 | 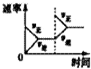 |  |
| A、A | B、B | C、C | D、D |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:由于该反应的正反应是体积减小的放热反应,所以增加压强平衡向正反应的方向移动;升高温度平衡向逆反应方向移动;增加反应物浓度平衡向正反应方向移动;催化剂对化学平衡的移动没有影响,但可以提高反应速率,据此判断.
解答:
解:A、根据先拐先平的原理,图中P2大于P1,而此时P2对应的氨气的体积分数小于P1,说明平衡逆向移动,与平衡移动原理相矛盾,故A错误;
B、该反应为放热反应,升高温度,平衡逆向移动,氮的转化率下降,故B错误;
C、增加氮气,反应物浓度增大,正反应速率增大,逆反应速率在开始的瞬间不变,平衡正向移动,故C正确;
D、有催化剂反应速率变快,反应到达平衡的时间变短,故D错误;
故选C.
B、该反应为放热反应,升高温度,平衡逆向移动,氮的转化率下降,故B错误;
C、增加氮气,反应物浓度增大,正反应速率增大,逆反应速率在开始的瞬间不变,平衡正向移动,故C正确;
D、有催化剂反应速率变快,反应到达平衡的时间变短,故D错误;
故选C.
点评:本题主要考查了影响平衡移动的因素,中等难度,解题时不注意对图象的观察,理清各个物理量的变化关系.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
用铂作电极电解下列溶液,一段时间后阴极产生的气体体积是阳极产生的气体的两倍的是( )
| A、NaOH |
| B、CuCl2 |
| C、HCl |
| D、CuSO4 |
某元素X的逐级电离能如图所示,下列说法正确的是( )


| A、X元素可能易形成X4+离子 |
| B、X可能VA族元素 |
| C、X为第五周期元素 |
| D、X与氯反应时可能生成XCl3 |
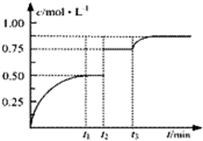 一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )
一定温度下,将1molA和1molB气体充入2L密闭容器,发生反应:A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示.下列说法正确是( )| A、t1~t3间该反应的平衡常数均为4 |
| B、反应方程式中的x=1 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量物质D |
X、Y、Z、W四种主族元素,若X的阳离子与Y的阴离子具有相同的电子层结构;W的阳离子的氧化性强于等电荷数的X阳离子的氧化性;Z阴离子半径大于等电荷数的Y的阴离子半径,下列说法不正确的是( )
| A、若W元素最高价氧化物对应的水化物为强碱,则X元素最高价氧化物对应的水化物不一定为强碱 |
| B、Y的氢化物比Z的氢化物更稳定 |
| C、原子序数:Z>X>Y>W |
| D、离子半径:Y>X |
下列做法中.不会造成大气污染的是( )
| A、燃烧含硫的煤 |
| B、焚烧树叶 |
| C、燃烧氢气 |
| D、燃放烟花爆竹 |
为了除去KCl固体中少量MgSO4和CaCl2杂质,须进行下列六项操作,①加水溶解②加热蒸发得到晶体③加入过量BaCl2溶液④加入过量盐酸⑤加入过量K2CO3⑥过滤.正确的次序是( )
| A、①⑤③⑥④② |
| B、①⑤③④⑥② |
| C、①③④⑥⑤② |
| D、①③⑤⑥④② |
 根据如图填空.
根据如图填空.