在水中加入等物质的量的AgNO3、Ba(NO3)2、NaCl、K2SO4,用惰性电极电解此溶液,通电片刻,则氧化产物与还原产物的质量比为( )
| A、8:1 |
| B、16:207 |
| C、71:2 |
| D、108:35.5 |
下列有关电解精炼铜的说法中错误的是( )
| A、粗铜做阴极 |
| B、电解一段时间后,溶液中会存在锌、铁等不活泼的金属阳离子 |
| C、阳极泥中含有金、银等贵重金属 |
| D、电解质溶液可以选用硫酸铜溶液 |
下列操作对配制的NaOH溶液浓度有偏高影响的是( )
| A、称量时将NaOH固体时用的砝码生锈 |
| B、将称量的NaOH固体置露在空气的时间过长 |
| C、选用的容量瓶内有少量的蒸馏水 |
| D、在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中 |
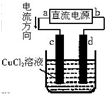 如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )| A、a为负极,b为正极 |
| B、a为阳极,b为阴极 |
| C、电解过程中,c电极质量减少、d电极质量增加 |
| D、如果阴极上有1.6 g铜析出,则阳极上产生气体的体积(标准状况)约为0.56 L |
取pH=4的某电解质溶液 1.00L,用 Pt电极进行电解,经过一段时间后,测得溶液的pH=1,且阴阳两极产物的物质的量之比为2:1,则该电解质溶液是( )
| A、盐酸 | B、氯化钾溶液 |
| C、硝酸银溶液 | D、硫酸铜溶液 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:下列叙述正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1. 实验测得起始、平衡时的有关数据如下表:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1. 实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A、反应的速率:③>①>② |
| B、达到平衡时氨气的浓度:①>② |
| C、放出的热量(kJ):a<b<92.4 |
| D、反应得到1mol NH3(l),放出热量46.2kJ |
 用如图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是( )
用如图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是( )