题目内容
在水中加入等物质的量的AgNO3、Ba(NO3)2、NaCl、K2SO4,用惰性电极电解此溶液,通电片刻,则氧化产物与还原产物的质量比为( )
| A、8:1 |
| B、16:207 |
| C、71:2 |
| D、108:35.5 |
考点:电解原理
专题:电化学专题
分析:等物质的量的这些离子加入到水中,Ag+和Cl-结合为AgCl沉淀,Ba2+ 和SO42-结合为BaSO4沉淀,溶液中就只有Na+、NO3-了,实际上是电解NaNO3溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气.
解答:
解:等物质的量的这些离子加入到水中,Ag+和Cl-结合为AgCl沉淀,Ba2+ 和SO42-结合为BaSO4沉淀,溶液中就只有K+、Na+、NO3-了,实际上是电解NaNO3溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气,当转移相同电子时,氧化产物和还原产物的质量之比为32:(2×2)=8:1,
故选:A.
故选:A.
点评:本题考查了电解池原理和离子共存,明确溶液中的溶质是解本题关键,很多学生只是根据离子放电顺序确定阴阳极上产物,因为漏掉了离子共存而导致错误,为易错题.

练习册系列答案
相关题目
2013年宿迁市政府提出创建国家级卫生城市,提出了“人人参与,创建绿色家园”口号.下列说法不正确的是( )
| A、回收废旧电池 |
| B、加强控制燃放烟花爆竹 |
| C、停止使用含铅汽油 |
| D、将工厂烟囱加高,减少周围大气污染 |
下列实验操作和结论错误的是( )
| A、用新制Cu(OH)2悬浊液可鉴别麦芽糖和蔗糖. |
| B、用银镜反应可证明蔗糖是否转化为葡萄糖,但不能证明是否完全转化. |
| C、采用盐析方法,可以分离提纯蛋白质 |
| D、蔗糖溶液中滴加几滴稀H2SO4,水浴加热几分钟,加入到银氨溶液中,水浴加热有银镜产生,证明蔗糖是还原性糖. |
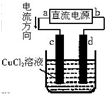 如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
如图是电解200mL 1mol?L-1 CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )| A、a为负极,b为正极 |
| B、a为阳极,b为阴极 |
| C、电解过程中,c电极质量减少、d电极质量增加 |
| D、如果阴极上有1.6 g铜析出,则阳极上产生气体的体积(标准状况)约为0.56 L |
恒温、恒压下,a mol A和b mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n mol C.则下列说法中正确的是( )
| A、物质A、B的转化率之比为a:b | ||
| B、当v正(A)=2v逆(B)时,可确定反应达到平衡 | ||
C、起始时刻和达到平衡后容器中的压强比为(a+b):(a+b-
| ||
| D、若起始时放入2a mol A和2b mol B,则达到平衡时生成2n mol C |
用下面的方案进行某些离子的检验,其中方案设计合理的是( )
A、检验SO42-:试液
| ||||
B、检验CO32-:试液
| ||||
C、检验Cl-:试液
| ||||
D、检验Fe2+:试液
|
能鉴别NaI、AgNO3、Na2CO3、NaAlO2四种溶液的试剂是( )
| A、NaClO |
| B、KOH |
| C、BaCl2 |
| D、HNO3 |
将Mg、Cu组成的2.64g混合物投入适量的浓硝酸中恰好反应,固体完全溶解使收集到的还原产物NO气体为0.896L(标准状况),向反应后溶液加入2mol/L的NaOH溶液至金属离子恰好完全沉淀.则形成的沉淀质量为( )
| A、4.32 g |
| B、4.68 g |
| C、5.36 g |
| D、6.38 g |
