某原子的基态电子排布为1s22s22p63s23p63d64s2,该元素不可能的价态是( )
| A、-1 | B、+2 | C、+3 | D、0 |
以下有关元素性质的说法不正确的是( )
| A、具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是① |
| B、具有下列价电子排布式的原子中,①3s23p1 ②3s23p2③3s23p3 ④3s23p4 第一电离能最大的是③ |
| C、①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ |
| D、某元素气态基态原子的逐级电离能(kJ?mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+ |
下列说法中正确的是( )
| A、所有的电子在同一区域里运动 |
| B、能量高的电子在离核远的区域运动,能量低的电子在离核近的区域运动 |
| C、处于最低能量的原子叫基态原子 |
| D、同一原子中,1s、2s、3s所能容纳的电子数越来越多 |
常温下,某澄清透明的溶液中可能存在:Fe2+、Cu2+、Mg2+、Al3+、SO32-、Br-、SO42-、NO3-等离子中的一种或几种,现进行了如下实验:

提示:SO32-与Al3+会发生双水解在水溶液中不能大量共存,SO32-与Fe2+、Cu2+、Mg2+会发生反应生成沉淀.
下列说法不正确的是( )

提示:SO32-与Al3+会发生双水解在水溶液中不能大量共存,SO32-与Fe2+、Cu2+、Mg2+会发生反应生成沉淀.
下列说法不正确的是( )
| A、沉淀B中可能含有氢氧化镁肯定含有氢氧化铁 |
| B、溶液中一定不存在SO32- |
| C、溶液中一定存在Fe2+、Al3+、Br-、SO42- |
| D、溶液中一定不存在Fe2+、Cu2+ |
原子核外每个电子层上均含有2n2个电子的元素是( )
| A、Be | B、C | C、Ar | D、Ne |
下列说法错误的是( )
| A、主族元素的原子核外电子最后填入的能级是s能级或p能级 |
| B、NH4+和CH4属于等电子体,立体构型都是正四面体 |
| C、BF3、NCl3、H2O分子中所有原子都满足最外层为8电子结构的是NCl3 |
| D、向盛有硫酸铜溶液的试管里加入过量氨水,将得到蓝色的Cu(OH)2沉淀 |
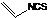 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3 【选做题--物质结构与性质】
【选做题--物质结构与性质】