可作为可逆反应 N2(g)+O2(g)?2NO(g)已达到平衡状态的标志的是( )
| A、单位时间内每生成 n mol N2,同时生成2 n mol NO |
| B、容器内反应混合物的总压强不随时间改变 |
| C、O2的消耗速率等于NO的消耗速率 |
| D、容器内始终有N2、O2和NO共存 |
室温下,某溶液中由水电离的c(H+)=10-13mol/L,下列各离子组在该溶液中一定不能大量共存的是( )
| A、NH4+、Cu2+、Cl-、NO3- |
| B、K+、Na+、SO32-、S2- |
| C、Ba2+、Fe2+、NO3-、Br- |
| D、K+、Na+、SO42-、AlO2- |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、酸性溶液中:Na+、K+、Fe3+、ClO- |
| B、溶液c(OH-)=10-12mol/L:NH4+、Al3+、NO3-、Cl- |
| C、某透明溶液:MnO4-、Mg2+、SO42-、Na+ |
| D、能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
| A、CO32-、OH-、Cl- |
| B、Cu2+、H+、Cl- |
| C、K+、H+、Cl- |
| D、K+、OH-、CO32- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0 mol?L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | ||
B、
| ||
| C、由水电离产生c (H+)=10-10mol/L的溶液:NH4+、AlO2-、Ca2+、S2- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:K+、SO32-、S2-、SO42- |
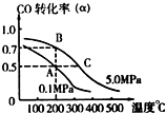 密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)=CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示.下列说法正确的是( )
密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)=CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示.下列说法正确的是( )| A、在 A、B两点对应的容器中,n(A)总:n(B)总=4:5 |
| B、在 A、C两点对应的容器中自反应开始到平衡状态所需的时间tA,<tC |
| C、设B、C两点的平衡常数分别为KB、KC,则KB<KC |
| D、在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率 |
下列有关金属冶炼的说法中,不正确的是( )
| A、用电解熔融氯化钠的方法得到活泼金属钠 |
| B、在加热的情况下利用氢气还原三氧化二铝得到金属铝 |
| C、用铝热反应原理炼得熔点较高的金属铬 |
| D、热分解法直接加热HgO得到金属Hg |
将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:
A(g)+B(g)?C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )
A(g)+B(g)?C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )

| A、反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是 0.225 mol?L-1?s-1 |
| B、该温度下,压缩气体体积至1L,反应的平衡常数增大 |
| C、恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行 |
| D、在上述反应体系中加入催化剂,化学反应速率增大,则E1和E2均减小 |
已知金属钾有如下性质:①钾的密度比水小;②钾的熔点低;③钾与水反应时放出热量;④钾与水反应后溶液呈碱性.某学生将一小块金属钾投入滴有酚酞溶液的水中,以上实验能证明上述四点性质中的( )
| A、①④ | B、①②④ |
| C、①③④ | D、①②③④ |