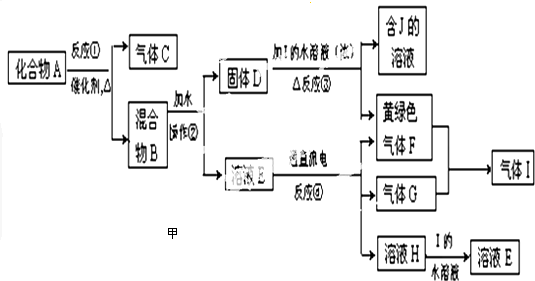
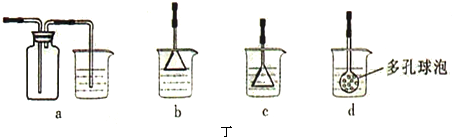
某强氧化剂XO(OH)2+被Na2SO3还原.如果还原2.4×10-3mol XO(OH)2+,需用30mL 0.2mol/L的Na2SO3溶液,那么X元素被还原后的价态是( )
| A、+2 | B、+1 | C、0 | D、-1 |
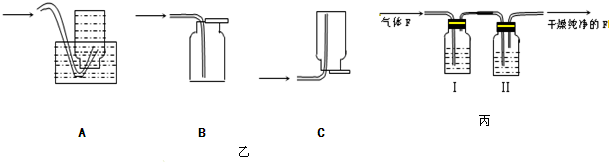
在蒸馏实验中,下列叙述不正确的是( )
A、在蒸馏烧瓶中盛约
| ||
| B、收集蒸馏水时,应弃去开始馏出的部分 | ||
| C、冷水从冷凝管下口入,上口出 | ||
| D、将温度计水银球插入自来水中 |
下列离子检验的方法正确的是( )
| A、某待测液加入AgNO3溶液,生成白色沉淀,说明原溶液中有Cl- |
| B、某待测液加入BaCl2溶液,生成白色沉淀,说明原溶液中有SO42- |
| C、某待测液加入CaCl2溶液,生成白色沉淀,说明原溶液中有CO32- |
| D、某待测液加入NaOH溶液,生成蓝色沉淀,说明原溶液中有Cu2+ |
粗食盐的杂质主要是MgCl2.为了除去杂质,工业上常把粗盐粉碎后用饱和食盐水浸洗,再过滤出食盐.对此,下面的评论正确的是( )
| A、浸洗前后,被浸洗的食盐中MgCl2的含量基本不变 |
| B、用来浸洗的饱和食盐水在浸洗前后没有变化 |
| C、浸洗用过的饱和食盐水可以无限次地使用下去 |
| D、粉碎颗粒的大小影响浸洗后盐中MgCl2的含量 |
合成氨的温度和压强通常控制在约500℃以及200~500atm的范围,且进入合成塔的N2和H2的体积比为1:3,经科学测定,在相应条件下,N2和H2反应所得氨的平衡浓度(体积分数)如下表所示.
而实际从合成塔出来的混合气体中含有氨约为15%,这表明( )
| 200atm | 600atm | |
| 500℃ | 19.1% | 42.2% |
| A、表中所测数据有明显误差 |
| B、生产条件控制不当 |
| C、氨的分解速率大于预测值 |
| D、合成塔中的反应并未达平衡 |
今有一混合物的水溶液,只可能含有以下离子中的若干种(不考虑水的电离):K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生;(2)第二份加足量NaOH溶液加热后,收集到标准状况下气体896ml(气体全部逸出);(3)第三份加足量BaCl2溶液后,得干燥沉淀6.3g,经足量盐酸洗涤、干燥后,沉淀质量4.66g.根据上述实验,以下推测正确的是( )
| A、K+一定存在 |
| B、100 mL溶液中含0.02 mol CO32- |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Mg2+可能存在 |