20世纪90年代,国际上提出了“预防污染”这一新概念.绿色化学是“预防污染”的基本手段.下列各项中属于绿色化学的是( )
| A、杜绝污染源 |
| B、减少有害物质 |
| C、治理污染点 |
| D、处理废弃物 |
将空气中氮气转化成氮的化合物的过程称为固氮.下列选项中能实现人工固氮的是( )
| A、闪电 | B、电解饱和食盐水车间 |
| C、根瘤菌 | D、合成氨车间 |
钙是人体必需的常量元素之一,下列关于钙的有关叙述不正确的是( )
| A、钙是人体内含量最丰富的元素之一 |
| B、在人体内钙构成骨骼和牙齿 |
| C、缺钙的人可以多喝牛奶、豆奶等乳制品补钙 |
| D、钙是人体内公认的“智慧元素” |
石灰石是许多工业的原料之一,但制取下列物质时不需用石灰石的是( )
| A、制硅 | B、制水泥 |
| C、制玻璃 | D、制生石灰 |
 某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.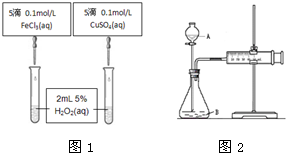
 学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.
学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.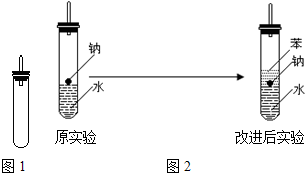

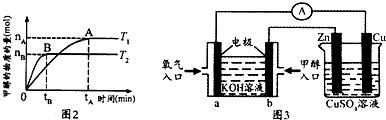
 某研究性学习小组探究NO3-在不同环境中的氧化性.
某研究性学习小组探究NO3-在不同环境中的氧化性.