题目内容
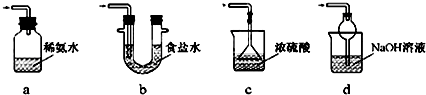
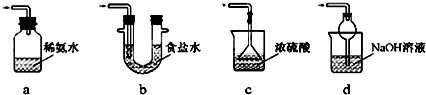
某实验小组对中学课本中可生成氢气的反应进行研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2,他们设计了如图1所示装置图,请回答下列问题:
(1)写出Na与H2O反应的离子方程式 .
(2)在点燃之前必须先进行 ,方法是 .
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了.他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少.于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是 .
(4)实验小组查阅钠、苯、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进如图2所示.在改进后的实验中的生成速率减慢.原因是 .

(1)写出Na与H2O反应的离子方程式
(2)在点燃之前必须先进行
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了.他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少.于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是
(4)实验小组查阅钠、苯、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进如图2所示.在改进后的实验中的生成速率减慢.原因是
考点:性质实验方案的设计,制备实验方案的设计
专题:实验设计题
分析:(1)钠和水反应生成氢氧化钠和氢气;
(2)可燃性气体与空气混合可能发生爆炸;氢气易燃烧,不纯氢气燃烧听到爆鸣声;
(3)大块的钠与水反应剧烈,放出大量的热;
(4)钠的密度比煤油大,比水小.
(2)可燃性气体与空气混合可能发生爆炸;氢气易燃烧,不纯氢气燃烧听到爆鸣声;
(3)大块的钠与水反应剧烈,放出大量的热;
(4)钠的密度比煤油大,比水小.
解答:
解:(1)钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,其离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)可燃性气体与空气混合可能发生爆炸,点燃前需要先验纯,检验方法为:用排水法收集一小试管氢气,用拇指堵住,管口向下移近火焰,松开手指,听到尖锐爆鸣声说明不纯,若声音很小,证明纯净;
故答案为:验纯;用排水法收集一小试管氢气,用拇指堵住,管口向下移近火焰,松开手指,听到尖锐爆鸣声说明不纯,若声音很小,证明纯净;
(3)大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸,
故答案为:大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸;
(4)钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止;
当钠表面的H2逸出,钠又回落水层,如此反复,减小了Na与H2O的反应速率,
故答案为:钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止;
当钠表面的H2逸出,钠又回落水层,如此反复,减小了Na与H2O的反应速率.
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)可燃性气体与空气混合可能发生爆炸,点燃前需要先验纯,检验方法为:用排水法收集一小试管氢气,用拇指堵住,管口向下移近火焰,松开手指,听到尖锐爆鸣声说明不纯,若声音很小,证明纯净;
故答案为:验纯;用排水法收集一小试管氢气,用拇指堵住,管口向下移近火焰,松开手指,听到尖锐爆鸣声说明不纯,若声音很小,证明纯净;
(3)大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸,
故答案为:大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸;
(4)钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止;
当钠表面的H2逸出,钠又回落水层,如此反复,减小了Na与H2O的反应速率,
故答案为:钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止;
当钠表面的H2逸出,钠又回落水层,如此反复,减小了Na与H2O的反应速率.
点评:本题考查常见气体制备原理及装置选择,题目难度不大,注意钠与水反应时,取用的钠块不能太大.注意(4)要考虑题给密度的关系,确定钠在反应体系中的位置关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列关于碳、硅及其化合物的叙述中,正确的是( )
| A、碳、硅都是较活泼的非金属,它们只能以化合态存在于自然界中 |
| B、等质量的Na2CO3、NaHCO3分别与足量盐酸反应,前者产生的CO2多 |
| C、一定条件下CO2、SiO2都能与NaOH、Na2CO3(或CaCO3)发生反应 |
| D、热稳定性:CH4<SiH4;酸性H2CO3>H2SiO3(H4SiO4) |
下列离子方程式书写正确的是( )
| A、过量二氧化碳通人偏铝酸钠溶液中:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32- | ||||
| B、氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O | ||||
| C、在碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ | ||||
D、碳酸氢铵溶液与过量的NaOH溶液混合:NH4++HCO3-+2OH-
|
钙是人体必需的常量元素之一,下列关于钙的有关叙述不正确的是( )
| A、钙是人体内含量最丰富的元素之一 |
| B、在人体内钙构成骨骼和牙齿 |
| C、缺钙的人可以多喝牛奶、豆奶等乳制品补钙 |
| D、钙是人体内公认的“智慧元素” |
某学生在一带活塞的密闭容器中装入1molNaHCO3和1molNa2O2,加热充分反应后容器内残留的固体是( )
| A、0.8molNa2CO3和0.6molNaOH |
| B、1molNa2CO3和1molNaOH |
| C、0.8molNa2CO3和1molNaOH |
| D、1molNa2CO3和0.6molNaOH |
下列有关实验操作中,正确的是( )
| A、用试管取出试剂瓶中的NaOH溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B、银镜反应实验后的废液可先倒入水槽中,再用水冲入下水道 |
| C、向试管中滴加液体时,胶头滴管必须紧贴试管内壁,避免液体溅出 |
| D、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为Zn+2OH--2e-=ZnO+H2O,Ag2O+2e-+H2O=2Ag+2OH-.椐此判断下列叙述中正确的是( )
| A、电池放电时,电池负极区溶液的碱性增强 |
| B、电池放电时,电子从Ag2O电极经外电路流向Zn电极 |
| C、Zn电极为负极,被氧化;Ag2O电极为正极,被还原 |
| D、Zn电极发生还原反应,Ag2O电极发生氧化反应 |