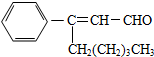 茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,关于茉莉醛的下列叙述正确的是( )
茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,关于茉莉醛的下列叙述正确的是( )| A、茉莉醛与苯甲醛互为同系物 |
| B、在加热和催化剂作用下加氢,每摩尔茉莉醛最多能消耗2mol氢气 |
| C、一定条件下,茉莉醛能被银氨溶液、新制氢氧化铜等多种氧化剂氧化 |
| D、从理论上说,202g茉莉醛能从足量银氨溶液中还原出216g银 |
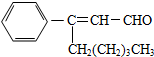 茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,关于茉莉醛的下列叙述正确的是( )
茉莉醛具有浓郁的茉莉花香,其结构简式如图所示,关于茉莉醛的下列叙述正确的是( )| A、茉莉醛与苯甲醛互为同系物 |
| B、在加热和催化剂作用下加氢,每摩尔茉莉醛最多能消耗2mol氢气 |
| C、一定条件下,茉莉醛能被银氨溶液、新制氢氧化铜等多种氧化剂氧化 |
| D、从理论上说,202g茉莉醛能从足量银氨溶液中还原出216g银 |