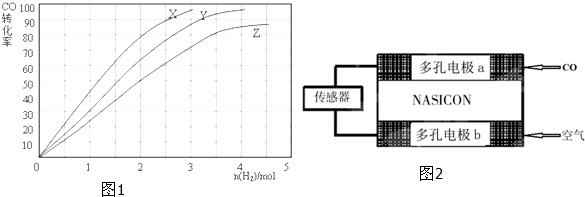
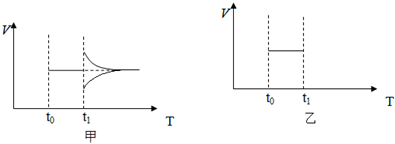
能增加反应物分子的活化分子的百分数,同时可以改变转化率的是( )
| A、升高温度 | B、使用催化剂 |
| C、增大压强 | D、增加浓度 |
向某4L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示.乙图为达到平衡后在t2、t3、t4、t5时改变某一种反应条件,平衡体系中速率随时间变化的情况,且所改变的条件均不同.已知t3-t4阶段为使用催化剂.则下列说法不正确的是( )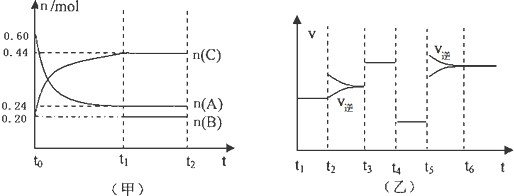

| A、若t1=15s,则t0-t1阶段以A浓度变化表示的反应速率v(A)为0.006mol/(L?s) |
| B、B的起始物质的量为0.08mol |
| C、若t2-t3阶段改变的条件是增大A的浓度,则平衡时C的体积分数变大 |
| D、该反应为放热反应 |
降低温度时,下列数据不一定减小的是( )
| A、化学反应速率v |
| B、溶度积常数Ksp |
| C、水解平衡常数Kh |
| D、水的离子积常数Kw |
已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(g)(正反应为放热反应),图中曲线a代表一定条件下该反应的过程,若使曲线a变为b曲线,可采取的措施是( )

| A、增大A的浓度 |
| B、缩小容器的体积 |
| C、加入催化剂 |
| D、升高温度 |
下列有关工业生产过程的叙述正确的是( )
| A、合成氨工业中及时将NH3液化分离,可加快反应速率,并提高N2、H2的转化率 |
| B、向汽油中添加甲醇后,该混合燃料的热值不变 |
| C、氯碱工业中采用阴离子交换膜法,可防止阴极产生的Cl2和阳极产生的碱反应 |
| D、目前淡化海水的方法有多种,其中蒸馏法历时最久,成本最高 |
足量铁片和100mL 5mol/L的稀H2SO4反应时,下列措施能加快H2的生成速率的是( )
| A、加入几滴CuSO4溶液 |
| B、加入少量6mol/L的稀盐酸 |
| C、升高温度 |
| D、不用稀硫酸,改用浓硝酸 |
在恒温、恒容的条件下,有反应2A(气)+2B(气)?C(气)+3D(气),现从两条途径分别建立平衡
途径I:A、B的起始浓度分别为2mol/L
途径Ⅱ:C、D的起始浓度分别为2mol/L 和6mol/L;则以下叙述中正确的是( )
途径I:A、B的起始浓度分别为2mol/L
途径Ⅱ:C、D的起始浓度分别为2mol/L 和6mol/L;则以下叙述中正确的是( )
| A、两途径最终达到平衡时,体系内混合气体各组分百分组成相同 |
| B、两途径最终达到平衡时,体系内混合气体各组分百分组成不同 |
| C、达到平衡时,途径I的反应速率等于途径Ⅱ的反应速率 |
| D、达到平衡时,途径I所得混合气的密度等于途径Ⅱ所得混合气密度 |