下列反应属于放热反应的是( )
| A、焦炭和二氧化碳共热 |
| B、NaOH溶于水 |
| C、KClO3受热分解 |
| D、CaO溶于水 |
下列规律与化学反应的能量变化关系最大的是( )
| A、阿伏加德罗定律 |
| B、盖斯定律 |
| C、勒夏特列原理 |
| D、欧姆定律 |
下列说法或表示方法中正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、由C(金刚石)═C(石墨)△H=-1.9kJ/mol 可知,金刚石比石墨稳定 |
| C、在101kpa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol |
| D、稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-53.7kJ/mol,若将含0.1mol 醋酸的溶液与含0.1 mol 氢氧化钠的溶液混合,放出的热量小于5.73kJ |
若A+酸→盐+水,则A不可能属于( )
| A、氧化物 | B、单质 | C、碱 | D、电解质 |
在2L容器中发生3A+B═2C的反应,最初加入的A、B都是4mol,10s 内A的反应速率为0.12mol/(L?s),10s后容器内B的物质的量浓度为( )
| A、1.6 mol/L |
| B、1.4 mol/L |
| C、3.2 mol/L |
| D、1.8 mol/L |
反应2SO2+O2?2SO3,经过10s O2的浓度增加了4mol/L,则用O2表示的反应速率为( )
| A、4 mol/(L?s) |
| B、0.4 mol/(L?s) |
| C、2 mol/(L?s) |
| D、0.2 mol/(L?s) |
100mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A、碳酸钠(固体) |
| B、石灰水 |
| C、硫酸钾溶液 |
| D、硫酸铵(固体) |
下列过程一定不能自发发生的是( )
| A、水从高处流向低处 |
| B、食盐溶解于水中 |
| C、水分解成H2和O2 |
| D、生石灰与水反应生成熟石灰 |
常温下,已知稀盐酸的物质的量浓度为a mol/L,稀NaOH溶液的物质的量浓度为b mol/L,当两种溶液等体积混合时,所得溶液的pH=2(混合液体积为原体积的和),则a和b的关系为( )
A、a=
| ||
B、b=
| ||
| C、a=b+0.1 | ||
| D、a=b+0.02 |
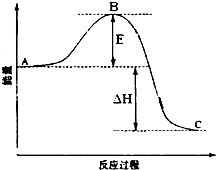 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题: