与3.2克SO2所含的氧原子数相等的NO2的质量为( )
| A、2.3 | B、4.6 |
| C、6.4 | D、3.2 |
下列化学用语正确的是( )
A、聚丙烯的结构简式: |
B、2-甲基-1-丁烯分子的键线式: |
C、四氯化碳分子的电子式: |
D、丙烷分子的比例模型: |
短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为32,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素.下列叙述正确的是( )
| A、四种元素的原子半径:A>B>C>D |
| B、最高价氧化物对应的水化物的酸性:B>D |
| C、C元素处于元素周期表中第3周期第ⅡA族 |
| D、B、D的最高价氧化物中,B、D与氧原子之间一定均为单键 |
铁、钴、镍的原子序数分别为26、27、28,它们的性质相似,被称为铁系元素.已知反应Fe2O3+6HCl=2FeCl3+3H2O,Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,则下列物质的氧化能力由强到弱的顺序是( )
| A、Fe2O3>Co2O3>Cl2 |
| B、Cl2>Fe2O3>Co2O3 |
| C、Cl2>Co2O3>Fe2O3 |
| D、Co2O3>Cl2>Fe2O3 |
0.5molH2SO4中大约含有( )
| A、0.5×6.02×1023 个H2SO4分子 |
| B、0.5×6.02×1023 个H2分子 |
| C、6.02×1023 个氢原子 |
| D、0.5×6.02×1023×50个质子 |
已知:①2Fe3++2I-=2Fe2++I2②2Fe2++Cl2=2Fe3++2Cl-③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O某溶液中含有Fe2+和I -,为了氧化I -而不使Fe2+被氧化,可选用的氧化剂是( )
| A、FeCl2 |
| B、KMnO4 |
| C、Cl2 |
| D、FeCl3 |
下列说法或表示正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定 |
| C、稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ |
| D、在101kPa时,H2燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol,则H2在101kPa时的燃烧热为571.6kJ/mol |
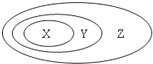 下表中所示物质或概念间的从属关系一定符合如图的是( )
下表中所示物质或概念间的从属关系一定符合如图的是( )