设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、1mol NaCl中,Na+的核外电子总数为10NA |
| B、1molFe与过量的稀HNO3反应,转移2NA个电子 |
| C、0.1mol?L?1Na2SO4液含有0.1NA个SO42- |
| D、常温常压下,22.4L氯气与足量镁粉充分反应,生成MgCl2 2NA |
下列溶液一定呈中性的是( )
A、c(OH-)=
| ||
| B、pH=7 的溶液 | ||
| C、c(H+)=10-14的溶液 | ||
| D、加甲基橙呈黄色的溶液 |
常温常压下,在等体积的密闭容器中充入下列气体后,压强最小的是( )
| A、0.3mol HCl和0.3molNH3 |
| B、0.2mol H2和0.1mol O2 |
| C、0.2mol NH3和0.1mol O2 |
| D、0.2mol N2和0.05mol H2 |
已知反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是( )


| A、电极X是正极,其电极反应为Cu-2e-=Cu2+ |
| B、银电极质量逐渐减小,Y溶液中c(Ag+)增大 |
| C、当X电极质量减少0.64g时,电解质溶液中有0.02mol电子转移 |
| D、外电路中电流计的指针有偏转 |




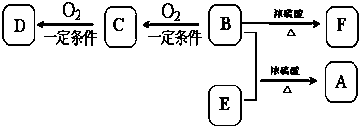
 基团.
基团. 将溶液(或气体)X逐渐加入(或通入)到一定量的Y溶液中,产生沉淀(或气体)的物质的量与加入X的物质的量关系如图所示,符合图中情况的一组物质是( )
将溶液(或气体)X逐渐加入(或通入)到一定量的Y溶液中,产生沉淀(或气体)的物质的量与加入X的物质的量关系如图所示,符合图中情况的一组物质是( ) SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如图所示实验装置.
SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如图所示实验装置.