0 129584 129592 129598 129602 129608 129610 129614 129620 129622 129628 129634 129638 129640 129644 129650 129652 129658 129662 129664 129668 129670 129674 129676 129678 129679 129680 129682 129683 129684 129686 129688 129692 129694 129698 129700 129704 129710 129712 129718 129722 129724 129728 129734 129740 129742 129748 129752 129754 129760 129764 129770 129778 203614
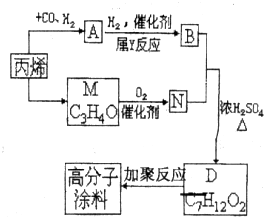 有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.