题目内容
在某合作课上,同学们对硫酸亚铁固体受热分解的产物提出了不同的观点(已知产物不超过3种):甲同学认为硫酸亚铁固体受热分解的产物是Fe2O3和SO3;乙同学认为硫酸亚铁固体受热分解的产物是Fe2O3、SO2和SO3;丙同学认为硫酸亚铁固体受热分解的产物是Fe2O3、SO2和O2.
(1)根据化学反应原理可知,上面三位同学中观点一定错误的是 (填“甲”、“乙”或“丙”),理由是 .
(2)为了探究硫酸亚铁固体受热分解的产物,丁同学查阅资料获得如下信息:SO2的熔点为-72℃,沸点为-10℃;SO3的熔点为16.8℃,沸点为44.8℃.该同学设计了如图装置进行实验.
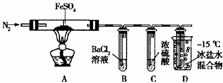
①加热之前通入氮气的目的是 .
②能否根据B中现象,判断硫酸亚铁分解一定有SO3生成?请你用必要的文字和化学方程式解释: .
③根据上述实验现象,可以肯定 (填“甲”、“乙”或“丙”)同学的观点一定正确.
④写出Ⅳ中发生反应的离子方程式: .
⑤设计一个简易实验检验A中硫酸亚铁是否完全分解: (写出步骤、现象和结论).
(1)根据化学反应原理可知,上面三位同学中观点一定错误的是
(2)为了探究硫酸亚铁固体受热分解的产物,丁同学查阅资料获得如下信息:SO2的熔点为-72℃,沸点为-10℃;SO3的熔点为16.8℃,沸点为44.8℃.该同学设计了如图装置进行实验.

| 实验过程 | 实验现象 | |
| Ⅰ | 通入一段时间N2加热 | A中固体变为红棕色,B中有白色沉淀生成,D试管中有无色液体生成 |
| Ⅱ | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| Ⅲ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| Ⅳ | 将重所得溶液滴入D试管中 | 混合溶液变为浅绿色 |
②能否根据B中现象,判断硫酸亚铁分解一定有SO3生成?请你用必要的文字和化学方程式解释:
③根据上述实验现象,可以肯定
④写出Ⅳ中发生反应的离子方程式:
⑤设计一个简易实验检验A中硫酸亚铁是否完全分解:
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:(1)依据氧化还原反应特征分析判断,反应前后元素化合价有升高,有降低分析判断;
(2)①加热之前通入氮气的目的是排出装置中的空气防止压强的氧化作用氧化硫酸亚铁;
②FeSO4分解不一定有SO3生成,B中的现象是有白色沉淀生成,可能是在水溶液中发生反应:2SO2+O2+2H2O=2H2SO4,H2SO4+BaCl2=BaSO4↓+2HCl,故无论分解反应是否有SO3 生成,都会有此现象;
③分解过程除产生使木条复燃的气体为氧气,A中固体变为红棕色为氧化铁,因为有Fe2O3生成,在FeSO4中只有+6价S元素有氧化性,能被还原,因此一定有SO2生成;
④A为氧化铁加盐酸生成三价铁离子,将所得溶液滴入D试管中,溶液变为浅绿色说明有二价铁生成,所以三价铁离子和二氧化硫发生了氧化还原反应,据此解答;
⑤取分解后的产物,加入盐酸溶解,利用亚铁离子的还原性分析,滴入高锰酸钾溶液若褪色证明分解完全;
(2)①加热之前通入氮气的目的是排出装置中的空气防止压强的氧化作用氧化硫酸亚铁;
②FeSO4分解不一定有SO3生成,B中的现象是有白色沉淀生成,可能是在水溶液中发生反应:2SO2+O2+2H2O=2H2SO4,H2SO4+BaCl2=BaSO4↓+2HCl,故无论分解反应是否有SO3 生成,都会有此现象;
③分解过程除产生使木条复燃的气体为氧气,A中固体变为红棕色为氧化铁,因为有Fe2O3生成,在FeSO4中只有+6价S元素有氧化性,能被还原,因此一定有SO2生成;
④A为氧化铁加盐酸生成三价铁离子,将所得溶液滴入D试管中,溶液变为浅绿色说明有二价铁生成,所以三价铁离子和二氧化硫发生了氧化还原反应,据此解答;
⑤取分解后的产物,加入盐酸溶解,利用亚铁离子的还原性分析,滴入高锰酸钾溶液若褪色证明分解完全;
解答:
解:(1)甲同学认为硫酸亚铁固体受热分解的产物是Fe2O3和SO3;依据氧化还原反应中元素化合价变化有升有降可知甲只有铁元素化合价升高,无元素化合价降低,不符合氧化还原反应的特征;乙同学认为硫酸亚铁固体受热分解的产物是Fe2O3、SO2和SO3;反应过程中有元素化合价升高和降低,符合氧化还原反应特征;丙同学认为硫酸亚铁固体受热分解的产物是Fe2O3、SO2和O2,反应 前后元素化合价有升高有降低,符合氧化还原反应特征;
故答案为:甲,甲得到的产物中元素化合价在反应前后只有升高无降低;
(2)①加热之前通入氮气的目的是排出装置中的空气防止压强的氧化作用氧化硫酸亚铁;
故答案为:赶净装置中的空气,避免空气中的氧气氧化硫酸亚铁干扰测定结果;
②因为硫酸亚铁在氮气的条件下隔绝空气加热分解一定生成氧化铁、二氧化硫,不一定有三氧化硫,B中的现象是有白色沉淀生成,白色沉淀为硫酸钡,该沉淀可能是2SO2+O2+2H2O=2H2SO4,H2SO4+BaCl2=BaSO4↓+2HCl,故无论分解反应是否有SO3 生成,都会有此现象,总反应为2SO2+O2+2H2O+2BaCl2=2BaSO4↓+4HCl,
故答案为:不正确,因为分解有O2 和SO2 生成,在水溶液中发生反应:2SO2+O2+2H2O=2H2SO4,故无论分解反应是否有SO3 生成,都会有此现象;2SO2+O2+2H2O+2BaCl2=2BaSO4↓+4HCl.
③根据氧化还原反应的特点,元素化合价升高的价数等于元素化合价降低的价数,分解过程除产生使木条复燃的气体为氧气说明氧元素的化合价在升高,A中固体变为红棕色为氧化铁,因为有Fe2O3生成,铁的化合价也在升高,在FeSO4中只有+6价S元素有氧化性,能被还原,因此一定有SO2生成,
故答案为:乙;
④取A中固体,加盐酸Fe2O3+6HCl=2FeCl3+3H2O,将所得溶液滴入D试管中,溶液变为浅绿色说明有二价铁生成,说明三价铁离子被还原,D试管中有无色液体为二氧化硫,发生的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
⑤取分解后的产物,加入盐酸溶解,利用亚铁离子的还原性分析,滴入高锰酸钾溶液若褪色证明分解完全,取少量分解产物与试管中,加入盐酸溶解后,滴入酸化的高锰酸钾溶液,若褪色,证明分解不完全,若紫红色不变化,证明分解完全;
故答案为:取少量分解产物与试管中,加入盐酸溶解后,滴入酸化的高锰酸钾溶液,若褪色,证明分解不完全,若紫红色不变化,证明分解完全;
故答案为:甲,甲得到的产物中元素化合价在反应前后只有升高无降低;
(2)①加热之前通入氮气的目的是排出装置中的空气防止压强的氧化作用氧化硫酸亚铁;
故答案为:赶净装置中的空气,避免空气中的氧气氧化硫酸亚铁干扰测定结果;
②因为硫酸亚铁在氮气的条件下隔绝空气加热分解一定生成氧化铁、二氧化硫,不一定有三氧化硫,B中的现象是有白色沉淀生成,白色沉淀为硫酸钡,该沉淀可能是2SO2+O2+2H2O=2H2SO4,H2SO4+BaCl2=BaSO4↓+2HCl,故无论分解反应是否有SO3 生成,都会有此现象,总反应为2SO2+O2+2H2O+2BaCl2=2BaSO4↓+4HCl,
故答案为:不正确,因为分解有O2 和SO2 生成,在水溶液中发生反应:2SO2+O2+2H2O=2H2SO4,故无论分解反应是否有SO3 生成,都会有此现象;2SO2+O2+2H2O+2BaCl2=2BaSO4↓+4HCl.
③根据氧化还原反应的特点,元素化合价升高的价数等于元素化合价降低的价数,分解过程除产生使木条复燃的气体为氧气说明氧元素的化合价在升高,A中固体变为红棕色为氧化铁,因为有Fe2O3生成,铁的化合价也在升高,在FeSO4中只有+6价S元素有氧化性,能被还原,因此一定有SO2生成,
故答案为:乙;
④取A中固体,加盐酸Fe2O3+6HCl=2FeCl3+3H2O,将所得溶液滴入D试管中,溶液变为浅绿色说明有二价铁生成,说明三价铁离子被还原,D试管中有无色液体为二氧化硫,发生的反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
⑤取分解后的产物,加入盐酸溶解,利用亚铁离子的还原性分析,滴入高锰酸钾溶液若褪色证明分解完全,取少量分解产物与试管中,加入盐酸溶解后,滴入酸化的高锰酸钾溶液,若褪色,证明分解不完全,若紫红色不变化,证明分解完全;
故答案为:取少量分解产物与试管中,加入盐酸溶解后,滴入酸化的高锰酸钾溶液,若褪色,证明分解不完全,若紫红色不变化,证明分解完全;
点评:本题考查了物质性质和分解产物的实验验证方法和过程理解应用,主要是氧化还原反应特征的分析应用,掌握基础是关键,题目难度较大.

练习册系列答案
相关题目
下列有关功能高分子材料中的高分子膜的用途,错误的是( )
| A、高分子分离膜可用于海水和苦咸水的淡化方面 |
| B、加热时,用高分子膜可浓缩天然果汁 |
| C、传感膜能够把化学能转化为电能 |
| D、热电膜能够把热能转换为电能 |
 如图为某有机物的结构简式,则等物质的量的该物质分别与Na,NaOH,NaHCO3反应是消耗的物质的量之比是( )
如图为某有机物的结构简式,则等物质的量的该物质分别与Na,NaOH,NaHCO3反应是消耗的物质的量之比是( )| A、4:2:1 |
| B、3:2:1 |
| C、1:1:1 |
| D、1:2:4 |