关于下列四个图象的说法中正确的是( )


| A、图①表示可逆反应CO(g)+H20(g)?5C02 (g)+H2(g)△H>0 |
| B、图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)影响,乙的压强大 |
| C、图③表示有无催化剂化学反应中能量变化 |
| D、图④表示C02通人饱和碳酸钠溶液中,溶液导电性变化 |
运用盖斯定律可方便地计算出难以通过实验直接测定的反应热.已知:
P4(白磷,s)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1
P(红磷,s)+
O2(g)=
P4O10(s)△H=-738.5kJ?mol-1
则白磷转化为红磷的热化学方程式为( )
P4(白磷,s)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1
P(红磷,s)+
| 5 |
| 4 |
| 1 |
| 4 |
则白磷转化为红磷的热化学方程式为( )
| A、P4(白磷,s)=4P(红磷,s)△H=-29.2kJ?mol-1 |
| B、P4(白磷,s)=4P(红磷,s)△H=+29.2kJ?mol-1 |
| C、P4(白磷,s)=4P(红磷,s)△H=-2244.7kJ?mol-1 |
| D、P4(白磷,s)=4P(红磷,s)△H=+2244.7kJ?mol-1 |
下列离子方程式书写正确的是( )
| A、将S02通入酸性KMnO4溶液:2MnO4-+5S02+2H20?2Mn2++5SO42-+4H+ |
| B、将Na2CO3溶液滴入等浓度等体积的盐酸中:C032-+H+?HCO3- |
| C、过氧化钠固体与水反应,2022-+2H20?40H-+02↑ |
| D、硫化钠水溶液呈碱性的原因:S2-+2H20?H2S+20H- |
化学反应伴随能量变化,下列说法中错误的是( )
| A、TNT(炸药)爆炸时部分化学能转化为热能 |
| B、电解饱和食盐水时部分化学能转化为电能 |
| C、镁条燃烧时部分化学能转化为光能 |
| D、植物光合作用时部分光能转化为化学能 |
下列反应过程中的能量变化符合如图情况的是( )
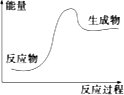

| A、酸与碱的中和反应 |
| B、Ba(OH)2?8H2O与NH4Cl的反应 |
| C、镁和盐酸的反应 |
| D、酒精燃烧 |
下列离子方程式书写正确的是( )
| A、将一小块钠投入水中Na+H2O=Na++OH-+H2↑ |
| B、硫酸和氢氧化钡混合Ba2++SO42-+H++OH-═BaSO4↓+H2O |
| C、F2和H2O的反应2F2+2H2O=4H++4F-+O2↑ |
| D、将少量NaOH溶液加入Ca(HCO3)2溶液中OH-+HCO3-+Ca2+=H2O+CaCO3↓ |
下列离子方程式的书写正确的是( )
| A、铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、NaHCO3溶液与NaOH溶液反应:OHˉ+HCO3ˉ═CO32ˉ+H2O |
| C、钠和冷水反应:Na+2H2O═Na++2OHˉ+H2↑ |
| D、氯气通入水中:Cl2+H2O═2H++Clˉ+ClOˉ |
锂-钒氧化物电池的能量密度远远超过其他材料电池,电池总反应式为xLi+V2O5
LixV2O5,下列说法正确的是( )
| 放电 |
| A、放电时,锂离子向负极移动 |
| B、放电时,负极上反应的物质是锂,正极上反应的物质是V2O5 |
| C、放电时,负极的电极反应为Li-e-=Li+ |
| D、充电时,V2O5在阴极被还原 |
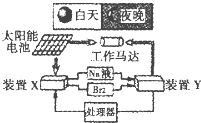 如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )
如图是设计的一种航天器能量储存系统原理示意图.它是利用太阳能和物质间的物质变化和能量转换实现循环使用.下列说法正确的是( )| A、二氧化硅是太阳能电池的光电转换材料 |
| B、装置X中阳极反应式:Br2+2e-2Br- |
| C、装置Y中正极反应式为:Br2+2e-2Br- |
| D、有了这套装置后就不用考虑节能减排了 |
下列有关电化学的叙述正确的是( )


| A、为实现铁上镀铜,可把铁作为阳极 |
| B、氯碱工业通过电解熔融的NaCl生产Cl2 |
| C、如图所示,盐桥中的K+移向ZnSO4溶液 |
| D、氢氧燃料电池(碱性电解质溶液)中O2通入正极,电极反应为O2+2H2O+4e-═4OH- |