题目内容
锂-钒氧化物电池的能量密度远远超过其他材料电池,电池总反应式为xLi+V2O5
LixV2O5,下列说法正确的是( )
| 放电 |
| A、放电时,锂离子向负极移动 |
| B、放电时,负极上反应的物质是锂,正极上反应的物质是V2O5 |
| C、放电时,负极的电极反应为Li-e-=Li+ |
| D、充电时,V2O5在阴极被还原 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:放电时,该原电池中锂失电子而作负极,V2O5得电子而作正极,负极上发生氧化反应,正极上发生还原反应,阳离子向正极移动,据此分析.
解答:
解:A.放电时,该装置是原电池,锂离子向正极移动,故A错误;
B.该原电池中,锂失电子而作负极,V2O5得电子而作正极,故B正确;
C.该原电池中,锂失电子发生氧化反应而作负极,电池反应式为:xLi-xe-=xLi+,故C正确;
D.放电时V2O5得电子而作正极,发生还原反应,充电时做阳极发生氧化反应,故D错误;
故选BC.
B.该原电池中,锂失电子而作负极,V2O5得电子而作正极,故B正确;
C.该原电池中,锂失电子发生氧化反应而作负极,电池反应式为:xLi-xe-=xLi+,故C正确;
D.放电时V2O5得电子而作正极,发生还原反应,充电时做阳极发生氧化反应,故D错误;
故选BC.
点评:本题考查原电池原理,明确元素化合价是解本题关键,根据得失电子来分析解答即可,难点是电极反应式的书写.

练习册系列答案
相关题目
下列物质属于强电解质的是( )
①HClO ②CH3COOH ③NaHCO3 ④CO2 ⑤酒精 ⑥H2SO4 ⑦CaCO3.
①HClO ②CH3COOH ③NaHCO3 ④CO2 ⑤酒精 ⑥H2SO4 ⑦CaCO3.
| A、①②④ | B、③⑥⑦ |
| C、②⑤⑦ | D、①③④⑥ |
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、1L 0.5mol?L-1氨水中所含NH4+数为0.5NA |
| B、1mol Fe与足量氯气反应转移的电子数为2 NA |
| C、标准状况下,33.6L CO2约含有1.5NA个分子 |
D、1 mol  中含碳碳双键数为3 NA 中含碳碳双键数为3 NA |
下列离子方程式与所述事实相符且正确的是( )
| A、CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO42-+2OH-+Ba2+═BaSO4↓+Cu(OH)2↓ |
| B、氯化铝溶液中加入过量的氨Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ |
| D、小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO2↑+H2O |
下列离子方程式书写正确的是( )
| A、将S02通入酸性KMnO4溶液:2MnO4-+5S02+2H20?2Mn2++5SO42-+4H+ |
| B、将Na2CO3溶液滴入等浓度等体积的盐酸中:C032-+H+?HCO3- |
| C、过氧化钠固体与水反应,2022-+2H20?40H-+02↑ |
| D、硫化钠水溶液呈碱性的原因:S2-+2H20?H2S+20H- |
下列有关电解质及氧化还原反应的叙述,正确的是( )
| A、某化合物溶于水导电,则该化合物为电解质 |
| B、NaCl溶液在电流作用下电离成Na+和Cl- |
| C、在氧化还原反应中,非金属单质一定是氧化剂 |
| D、元素由化合态变成游离态时,它可能被氧化,也可能被还原 |
碘元素的一种核素
I可用于治疗肿瘤.下列有关碘元素的说法正确的是( )
125 53 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
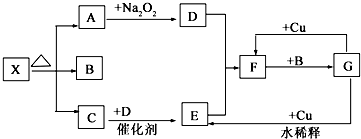 如图的各方框表示有关的一种反应物或生成物(某些物质已略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,X中阴阳离子个数相等.
如图的各方框表示有关的一种反应物或生成物(某些物质已略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,X中阴阳离子个数相等.