对水的电离平衡不产生影响的粒子是( )
| A、Fe3+ |
| B、Cl- |
| C、CH3COOH |
| D、NH3?H2O |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体与原溶质相同的是( )
| A、FeCl3溶液 |
| B、NaHCO3溶液 |
| C、Na2SO3溶液 |
| D、Na2SO4溶液 |
能使反应Cu+H2O═Cu(OH)2+H2↑发生的是( )
| A、用铜片作阴、阳电极,电解硫酸钾溶液 |
| B、用铜片作阴、阳电极,电解氯化铜溶液 |
| C、铜锌合金在潮湿空气发生电化学腐蚀 |
| D、铜片作原电池的负极,碳棒作原电池的正极,稀硫酸作电解质溶液 |
关于如图所示装置的叙述,正确的是( )
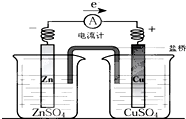

| A、铜是阳极,铜片上有气泡产生 |
| B、正极附近的SO42-离子浓度逐渐增大 |
| C、电流从锌片经导线流向铜片 |
| D、铜离子在铜片表面被还原 |
 同学用电解原理设计一个观察Fe(OH)2沉淀和Fe(OH)2被氧化的实验装置.如图所示,有关该装置的说法正确的是( )
同学用电解原理设计一个观察Fe(OH)2沉淀和Fe(OH)2被氧化的实验装置.如图所示,有关该装置的说法正确的是( )| A、断开K2,接通K1,铁棒和石墨棒上都放出大量气泡,两电极附近溶液颜色均无变化 |
| B、断开K2,接通K1,仅石墨捧上放出大量气泡,石墨电极附近溶液变红,一段时间后水槽中可见白色沉淀生成且保持较长时间不变色 |
| C、断开K2,接通K1,一段时间后再断开K1,接通K2,由于苯层的保护作用,白色沉淀仍能长时间保持不变色 |
| D、若先断开K1,接通K2,铁棒和石墨棒上都放出大量气泡,石墨电极附近溶液变红 |
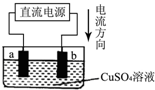 化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )
化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )| A、a是电解池的阴极、b是电解池的阳极 |
| B、b电极上的电极反应为:4OH--4e-=2H2O+O2↑ |
| C、通电一段时间后,溶液的PH减小 |
| D、通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的CuSO4 |
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1mol氢气的化学键消耗的能量为Q1kJ,破坏1mol氯气的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,下列关系式正确的是( )
| A、Q1+Q 3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2<2Q3 |
2014年6月5日为世界环境日,主题为“提高你的呼声而不是海平面”,提倡节能减排,以下措施中不能体现这一思想的是( )
| A、在电解铝工业中添加冰晶石 |
| B、研制出性能优良的催化剂,降低反应所需温度 |
| C、开发太阳能、风能、氢能等清洁能源 |
| D、大力发展火电,缓解用电紧张 |
对于复分解反应:X+Y=Z+W,下列叙述正确的( )
| A、若Z是强酸,则X或Y必有一种是酸 |
| B、若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
| C、若W是弱碱,Z是盐,则X或Y必有一种是强碱 |
| D、若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
如图是电解CuCl2溶液的装置,c、d为石墨电极,下列有关的判断正确的是( )
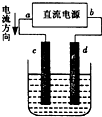

| A、电解过程中,d电极质量增加 |
| B、a为阳极、b为阴极 |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度基本不变 |