下列有关实验误差分析中,不正确的是( )
| A、用湿润的pH试纸测稀碱液的pH值,测定值偏小 |
| B、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C、滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
| D、测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低 |
物质的量浓度相同的下列溶液中,NH4+浓度最大的是( )
| A、NH4Cl |
| B、NH4HCO3 |
| C、CH3COONH4 |
| D、NH4HSO4 |
下列实验误差分析错误的是( )
| A、用湿润的pH试纸测稀碱溶液的pH,测定值偏小 |
| B、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C、滴定前滴定管尖嘴内有气泡,终点读数时尖嘴内无气泡,所测体积偏大 |
| D、测定1mol气体体积时,未冷却至室温就读数,所测体积偏大 |
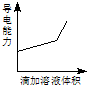 浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )| A | B | C | D | |
| 溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
| 溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
| A、A | B、B | C、C | D、D |
向含有Fe2+,Al3+,NH4+,Na+,K+的溶液中加入过量的Na2O2固体,微热溶液使其充分反应,再通入过量的HCl气体,则反应后溶液中离子浓度大量减小的是( )
| A、Na+和K+ |
| B、Al3+和Na+ |
| C、Fe2+和NH4+ |
| D、Fe2+和K+ |
室温下,将一元酸HA溶液和NaOH溶液等体积混合(忽略体积变化),实验数据如下表下列判断正确的是( )
| 实验编号 | 起始浓度(mol/L) | 反应后溶液的pH | |
| C(HA) | C(NaOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A、实验①反应后的溶液中C(Na+)>C(A-)>C(OH-)>C(H+) | ||
B、实验①反应后的溶液中C(OH-)=C(Na+)-C(A-)=
| ||
| C、实验②反应后的溶液中C(A-)+C(HA)=0.1 mol/L | ||
| D、实验②反应后的溶液中C(Na+)=C(A-)>C(OH-)=C(H+) |
下列有关物质性质的说法错误的是( )
| A、结合质子能力:ClO->HCO3->SiO32- |
| B、离子半径:F->Na+>Be2+ |
| C、还原性:H2S>HCl>HF |
| D、热稳定性:H2O>H2S>PH3 |
下列关于电解质溶液中离子关系的说法正确的是( )
| A、0.1mol?L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、0.1mol?L-1NH4Cl和0.1mol?L-1NH3?H2O等体积混合后离子浓度关系:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-) |
| D、常温下,在pH=1的溶液中,Fe2+、NO3-、ClO-、Na+能大量共存 |
对于常温下pH为2的盐酸,叙述不正确的是( )
| A、c(H+)=c(Cl-)+c(OH-) |
| B、与等体积pH=12的氨水混合后所得溶液显碱性 |
| C、由H2O电离出的c(H+)=1.0×10-12 mol?L-1 |
| D、与等体积0.01 mol?L-1醋酸钠溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |