AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,则下列说法不正确的是( )
| A、A不是ⅢA族元素 |
| B、AB3可以是三氧化硫 |
| C、B原子比A原子多10个电子 |
| D、B的氢化物和A的氢化物都极易溶于水 |
某溶液中除水电离出的离子外只可能含有Na+、Ba2+、Cl-、Br-、SO32-、SO42-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:下列结论正确的是( )
| 步骤 | 操作 | 现象 |
| (1) | 25℃时,用pH试纸检验 | 溶液pH大于7 |
| (2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| (3) | 向(2)所得的水溶液中加入稀HNO3和Ba(NO3)2溶液 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加入稀HNO3和AgNO3溶液 | 有白色沉淀产生 |
| A、肯定含有的离子是Na+、SO32-、Br-、Cl- |
| B、肯定含有的离子是SO32-、Br-、Cl- |
| C、不能确定的离子是Na+、Cl-、SO42- |
| D、不能确定的离子是Cl-、SO42- |
下列装置所示的实验中,能达到实验目的是( )
A、 分离碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、 除去Cl2中的HCl |
D、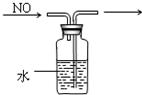 排水集气法收集NO |
实验室制备Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O 反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20mL反应残余液进行实验),其中正确的是( )
| ||
| A、与足量AgNO3溶液反应,过滤、洗涤、干燥,称量生成的沉淀质量为a g |
| B、稀释10倍后取20 mL用已知浓度的NaOH溶液滴定,消耗NaOH的体积为b mL |
| C、与足量NaHCO3固体反应,逸出气体用足量碱石灰吸收,增重c g |
| D、加入d1g CaCO3(过量)充分反应后,称量剩余固体质量为d2 g[已知:Ksp( CaCO3)>Ksp( MnCO3)] |
为检验Na2SO4溶液中是否混有NaCl,下列方法正确的是( )
| A、加入AgNO3溶液和稀HNO3,看是否有浑浊出现 |
| B、加入BaCl2溶液和稀HCl,看是否有浑浊出现 |
| C、先加过量的BaCl2溶液和稀HNO3,取上层清液再加AgNO3溶液,看是否有浑浊出现 |
| D、先加过量的Ba(NO3)2溶液和稀HNO3,取上层清液再加AgNO3溶液,看是否有浑浊出现 |




