题目内容
AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,则下列说法不正确的是( )
| A、A不是ⅢA族元素 |
| B、AB3可以是三氧化硫 |
| C、B原子比A原子多10个电子 |
| D、B的氢化物和A的氢化物都极易溶于水 |
考点:原子结构与元素的性质
专题:
分析:AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,据此推断A应为N元素,B应为Cl元素,据此选择即可.
解答:
解:A、依据分析可知A为氮元素,不是ⅢA族元素,故A正确;
B、依据分析可知AB3是NCl3,不可能是SO3,若为SO3,那么A原子比B原子多一个电子层,不符合题意,故B错误;
C、B为Cl,电子数为17,A为N,电子数为7,故B比A多10个电子,故C正确;
D、B的氢化物HCl和A的氢化物NH3均是易溶于水的,故D正确,故选B.
B、依据分析可知AB3是NCl3,不可能是SO3,若为SO3,那么A原子比B原子多一个电子层,不符合题意,故B错误;
C、B为Cl,电子数为17,A为N,电子数为7,故B比A多10个电子,故C正确;
D、B的氢化物HCl和A的氢化物NH3均是易溶于水的,故D正确,故选B.
点评:本题考查了元素位置、结构、性质的相互关系及应用,正确推断元素是解本题关键,结合原子、离子的结构来分析解答,难度中等.

练习册系列答案
相关题目
下列各组物质不易用物理性质区别的是( )
| A、苯和四氯化碳 |
| B、酒精和汽油 |
| C、碘和高锰酸钾固体 |
| D、氯化铵和硝酸铵晶体 |
下列装置所示的实验中,能达到实验目的是( )
A、 分离碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、 除去Cl2中的HCl |
D、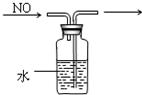 排水集气法收集NO |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)
2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
| V2O5 |
| 450℃ |

| A、图Ⅰ表示的是温度对化学平衡的影响,且乙的温度较高 |
| B、图Ⅱ表示的是t1时刻充入气体氦后对反应速率的影响 |
| C、图Ⅲ表示的是升高温度对反应速率的影响 |
| D、图Ⅲ表示的是t1时刻增大O2的浓度对反应速率的影响 |
下列溶液中Cl-的物质的量与100mL 2mol?L-1MgCl2溶液中Cl-的物质的量相等的是( )
| A、150 mL 4 mol?L-1 NaCl溶液 |
| B、75 mL 1 mol?L-1 AlCl3溶液 |
| C、50 mL 2 mol?L-1 CaCl2溶液 |
| D、200 mL 2 mol?L-1 KCl溶液 |
 的同分异构体有多种,同时满足下列条件的A的同分异构体有( )种.
的同分异构体有多种,同时满足下列条件的A的同分异构体有( )种.