题目内容
下列装置所示的实验中,能达到实验目的是( )
A、 分离碘酒中的碘和酒精 |
B、 实验室制氨气 |
C、 除去Cl2中的HCl |
D、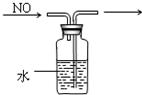 排水集气法收集NO |
考点:化学实验方案的评价
专题:
分析:A.碘和酒精不分层;
B.氯化铵分解生成氨气和氯化氢,在温度稍低时又生成氯化铵;
C.二者都与氢氧化钠反应;
D.NO不溶于水,可用排水法收集.
B.氯化铵分解生成氨气和氯化氢,在温度稍低时又生成氯化铵;
C.二者都与氢氧化钠反应;
D.NO不溶于水,可用排水法收集.
解答:
解:A.碘易溶于酒精,应用蒸馏的方法分离,故A错误;
B.氯化铵分解生成氨气和氯化氢,在温度稍低时又生成氯化铵,实验室应用氯化铵和氢氧化钙在加热条件下制备氨气,故B错误;
C.二者都与氢氧化钠反应,应用饱和食盐水除杂,故C错误;
D.NO不溶于水,可用排水法收集,故D正确.
故选D.
B.氯化铵分解生成氨气和氯化氢,在温度稍低时又生成氯化铵,实验室应用氯化铵和氢氧化钙在加热条件下制备氨气,故B错误;
C.二者都与氢氧化钠反应,应用饱和食盐水除杂,故C错误;
D.NO不溶于水,可用排水法收集,故D正确.
故选D.
点评:本题考查较为综合,涉及物质的分离和制备,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
已知短周期主族元素X、Y、Z、W、R,其中X的原子半径在短周期主族元素中最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W与Z同主族,R元素原子与Y元素原子的核外电子数之比为2:l.下列叙述错误的是( )
| A、X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 |
| B、Z、W、R最高价氧化物对应水化物的酸性:R>W>Z |
| C、RY2、WY2通入BaCl2溶液中均有白色沉淀生成 |
| D、Y的氢化物比R的氢化物稳定,且熔沸点高 |
下列实验方法能达到实验目的是( )
| A、用淀粉溶液检验溶液中是否存在碘单质 |
| B、用分液漏斗分离水与乙醇的混合物 |
| C、用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 |
| D、用硝酸银溶液检验某溶液中是否含有氯离子 |
AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,则下列说法不正确的是( )
| A、A不是ⅢA族元素 |
| B、AB3可以是三氧化硫 |
| C、B原子比A原子多10个电子 |
| D、B的氢化物和A的氢化物都极易溶于水 |
下列有关实验的说法正确的是( )
| A、制氯气时,用饱和碳酸钠溶液和浓硫酸净化气体 |
| B、制少量氧化钠时,将钠置于纯氧中燃烧 |
| C、制二氧化硫时,用浓硫酸干燥气体 |
| D、配制氢氧化钠溶液时,称取一定质量氢氧化钠固体放人容量瓶中并加水至刻度线 |
已知:2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是( )
| ||
| A、有BaSO4生成 |
| B、有BaSO3生成 |
| C、同时有BaSO4和BaSO3生成 |
| D、有SO3逸出 |
下列表述正确的一组是( )
| A、16O与18O互为同位素;H2、D2、T2互为同素异形体 |
| B、过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同;互为同分异构体 |
| C、P4、CH4、NH4+粒子的空间构型均为正四面体型;CO2、CS2均为直线型分子 |
D、Ca2+的离子结构示意图为 ,NH4Cl的电子式为 ,NH4Cl的电子式为 |