下列离子方程式正确的是( )
| A、向Mg( HC03)2溶液中加入过量的NaOH溶液:Mg2++2 HC03-+20H-═MgC03↓+C032-+2H20 |
| B、向NH4 Al( S04)2溶液中滴人Ba( OH)2溶液使SO42-反应完全:2Ba2++40H-十Al3++2 SO42-═2BaS04↓+Al02-+2H20 |
| C、足够的C02通入饱和碳酸钠溶液中:C02+CO32-+H20=2 HC03- |
| D、向Fe( N03)2溶液中加入稀盐酸:3Fe2++4H++N03-═3Fe3++NO↑+2H20 |
设NA为阿伏伽德罗常数的值,下列有关NA的说法正确的是( )
| A、标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
| B、将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA |
| C、1 mol Fel2与足量氯气反应时转移的电子数为2NA |
| D、标准状况下,560ml的CH4和甲醛的混合气体,含有的共用电子对数为0.1NA |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、一定条件下,l mol N2与足量H2反应生成NH3,转移电子6NA |
| B、标准状况下,11.2 L CCl4中含有C-Cl键的数目为2NA |
| C、1 mol甲基(-14C1H3)含有的中子数和电子数分别为8NA、9NA |
| D、1 mol?L-1Na2CO3溶液中含有的钠离子总数为2NA |
元素周期律揭示元素间的递变规律既有相似性又有递变性,下列递变规律正确的是( )
| A、第二周期元素氢化物稳定性的顺序是:HF>H2O,所以第三周期元素氢化物稳定性的顺序也是:HCl>H2S |
| B、IVA族元素氢化物熔点顺序是:SiH4>CH4,所以VA族元素氢化物熔点顺序也是:PH3>NH3 |
| C、第三周期元素的非金属性:Cl>S,所以其对应的氢化物水溶液的酸性也是:HCl>H2S |
| D、钠比铝活泼,工业上用电解熔融氯化钠制备钠,所以工业上也用电解熔融氯化铝制备铝 |
下列是一些化学键的键能:
根据键能数据估算:CH4 (g)+4F2 (g)=CF4(g)+4HF(g),该反应每生成1molHF(g)( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ?mol-1) | 414 | 489 | 565 | 155 |
| A、放热485 kJ |
| B、吸热485 kJ |
| C、放热1940 kJ |
| D、吸热1940 kJ |
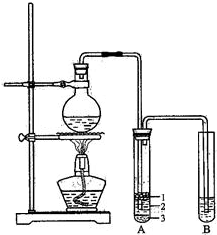 根据题意完成下列填空:有关数据列表如下:
根据题意完成下列填空:有关数据列表如下: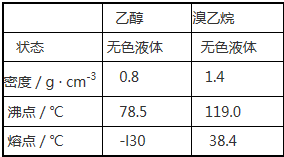
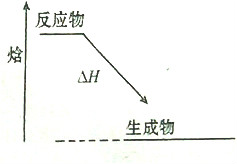
 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.