题目内容
如图为某反应的焓变示意图,下列有关反应符合该图象的是( )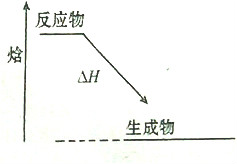
①CO加热分解为C和O2
②Mg+2HCl═MgCl2+H2↑
③H-Cl═H+Cl
④氢氧化亚铁被氧化成氢氧化铁.

①CO加热分解为C和O2
②Mg+2HCl═MgCl2+H2↑
③H-Cl═H+Cl
④氢氧化亚铁被氧化成氢氧化铁.
| A、① | B、④ | C、①③ | D、②④ |
考点:反应热和焓变
专题:
分析:依据图象分析焓变变化是能量的变化,反应物能量高于生成物能量,反应的焓变△H=生成物总焓-反应物总焓<0是放热反应,据此分析判断.
解答:
解:①CO加热分解为C和O2,为碳与氧气燃烧生成一氧化碳的逆反应,则为吸热反应,故错误;
②Mg+2HCl═MgCl2+H2↑,为放热反应,故正确;
③H-Cl═H+Cl为断键吸热过程,故错误;
④氢氧化亚铁被氧化成氢氧化铁,为放热反应,故正确;
故选D.
②Mg+2HCl═MgCl2+H2↑,为放热反应,故正确;
③H-Cl═H+Cl为断键吸热过程,故错误;
④氢氧化亚铁被氧化成氢氧化铁,为放热反应,故正确;
故选D.
点评:本题考查了化学反应的能量变化分析,注意图象中物质能量变化是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列溶液中有关物质的浓度关系正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl) |
| B、等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
可以充分说明反应P(g)+Q(g)?R(g)+S(g)在恒温下已达到平衡的是( )
| A、反应容器内的压强不随时间改变 |
| B、反应容器内P、Q、R、S四者浓度之比为1:1:1:1 |
| C、P的生成速率和S的生成速率相等 |
| D、反应容器内的气体总物质的量不随时间变化 |
元素周期律揭示元素间的递变规律既有相似性又有递变性,下列递变规律正确的是( )
| A、第二周期元素氢化物稳定性的顺序是:HF>H2O,所以第三周期元素氢化物稳定性的顺序也是:HCl>H2S |
| B、IVA族元素氢化物熔点顺序是:SiH4>CH4,所以VA族元素氢化物熔点顺序也是:PH3>NH3 |
| C、第三周期元素的非金属性:Cl>S,所以其对应的氢化物水溶液的酸性也是:HCl>H2S |
| D、钠比铝活泼,工业上用电解熔融氯化钠制备钠,所以工业上也用电解熔融氯化铝制备铝 |
下列相关的离子方程式书写正确的是( )
| A、NaHS溶液显碱性:HS-+H2O?S2-+H3O+ |
| B、向Ca(C1O)2溶液中通入SO2:SO2+2ClO-+H2O=SO32-+2HClO |
| C、硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、向氯化铝溶液中加入适量氨水:Al3++3NH3?H2O=3NH4++Al(OH)3↓ |
常温下,K(CH3COOH)>K1(H2CO3)>K(HClO)>K2(HCO3-)下列离子方程式书写正确的是( )
| A、向碳酸钠溶液中滴加少量醋酸:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O |
| B、向次氯酸钠溶液中通入少量CO2:2ClO-+H2O+CO2═2HClO+CO32- |
| C、向醋酸清洗水垢后氢氧化镁:2CH3COOH+Mg(OH)2═Mg2++2CH3COO-+2H2O |
| D、向漂白粉溶液中通入少量的SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |

 表示一些物质间的从属关系,不正确的是( )
表示一些物质间的从属关系,不正确的是( )