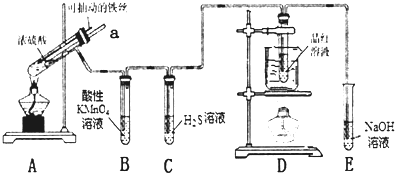
用18mol/L H2SO4溶液和100mL容量瓶配置1.8mol/L H2SO4溶液,下列有关说法正确的是( )
| A、将10mL 18mol/L H2SO4溶液加入盛有90mL水的容量瓶中 |
| B、将10mL 18mol/L H2SO4溶液加入容量瓶中,加水至刻度线 |
| C、加水时不慎超过刻度线,立即用胶头滴管吸出多余液体 |
| D、定容时仰视刻度线,配置的溶液浓度偏小 |
某有机物A(C8H16O2)能发生如图所示的变化,其中C与F是同分异构体.则符合条件的有机物A有多少种( )

| A、1种 | B、2种 | C、3种 | D、4种 |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已吸潮 |
| B、容量瓶未干燥 |
| C、烧杯内有少量NaOH溶液残留 |
| D、定容时俯视液面 |
已知反应2A(g)?2B(g)+C(g)△H<0,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为( )
| A、减小容器容积 |
| B、增大容器容积 |
| C、减小B的浓度 |
| D、降温 |
在一定温度下的定容密闭容器中,当下列物理量不再变化时,不能表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A、B的物质的量浓度 |
| B、混合气体的密度 |
| C、混合气体的平均相对分子质量 |
| D、混合气体的压强 |
配制0.50mol?L-1的NaOH溶液245ml,下列操作正确的是( )
| A、用托盘天平称取4.9gNaOH固体 |
| B、NaOH固体加蒸馏水溶解,要待溶液冷却到室温后,再转移至容量瓶中 |
| C、容量瓶不能用玻璃瓶塞、应用塑料瓶塞 |
| D、定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
下列有关实验的说法正确的是( )
| A、加入Cu粉可以除去FeSO4溶液中的Fe2(SO4)3 |
| B、取少量溶液X,向其中加入适量新制氯水,再加入几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C、用容量瓶配制1.00mol/L的NaOH溶液,定容时俯视刻度线,会使配出的溶液浓度偏大 |
| D、由于SiO2能与NaOH溶液反应,故NaOH溶液不能用玻璃瓶瓶盛放 |
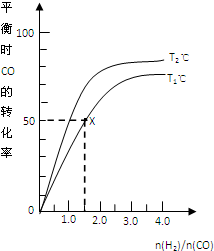 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)CH3OH(g)△H<0有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)CH3OH(g)△H<0有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 | ||
C、同一温度下,
| ||
D、相同条件下
|