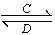几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
元素 代号 | A | B | D | E | G | H | I | J |
化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A.I在DB2中燃烧生成两种化合物
B.A、H、J的离子半径由大到小顺序是H>J>A
C.G元素的单质不存在同素异形体
D.B和J能形成既含离子键又含共价键的化合物
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如下图。下列说法正确的是( )
| X |
| Y |
|
|
|
| W |
|
|
|
|
|
|
A.五种元素中,原子半径最大的是W
B.Y与Z形成的化合物都可以和盐酸反应
C.Y的简单阴离子比W的简单阴离子还原性强
D.Z与Q形成的化合物水溶液一定显酸性
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
化合价 | -4 | +1 | -4 | -2 | -1 |
A.乙的常见氧化物只有一种
B.气态氢化物稳定性:丙>丁
C.丙的氧化物能与戊的氢化物的水溶液反应
D.原子半径大小:戊<丙
A、B、D、E四种元素均为短周期元素,原子序数逐渐增大。A元素原子的核外电子数、电子层数和最外层电子数均相等。B、D、E三种元素在周期表中的相对位置如图①所示,只有E元素的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子含有10个电子。它们之间的转化关系如图②所示。
B | D |
|
|
| E |
图①
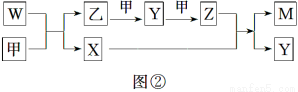
请回答下列问题:
(1)Z的化学式为__________________。
(2)E的单质与水反应的离子方程式为________________________________________。
(3)W?空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W?空气燃料电池放电时,正极反应式为________________________________,负极反应式为____________________。
(4)将一定量的A2、B2的混合气体放入1 L密闭容器中,在500 ℃、2×107 Pa下达到平衡。测得平衡气体的总物质的量为0.50 mol,其中A2为0.3 mol,B2为0.1 mol。则该条件下A2的平衡转化率为________,该温度下的平衡常数为____________(结果保留3位有效数字)。