0 109296 109304 109310 109314 109320 109322 109326 109332 109334 109340 109346 109350 109352 109356 109362 109364 109370 109374 109376 109380 109382 109386 109388 109390 109391 109392 109394 109395 109396 109398 109400 109404 109406 109410 109412 109416 109422 109424 109430 109434 109436 109440 109446 109452 109454 109460 109464 109466 109472 109476 109482 109490 203614
 冷却
冷却
 出现白色沉淀
出现白色沉淀
 溶液变蓝色
溶液变蓝色
 重结晶
重结晶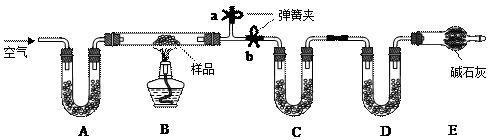
 网
网
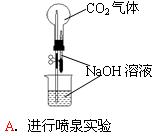
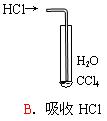
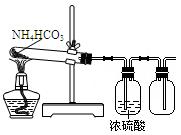
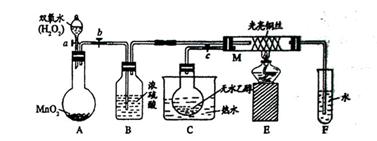
 Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。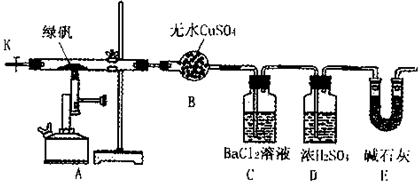

 、
、 、
、 等物质,
等物质, 和
和 [一直
[一直 是两性氢氧化物且溶解于氨水],并且填写下列实验报告。
是两性氢氧化物且溶解于氨水],并且填写下列实验报告。