题目内容
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
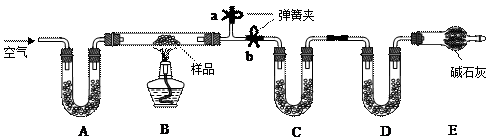
⑴加热前通入空气的目的是____ ___,操作方法为______________________________________________。
⑵装置A、C、D中盛放的试剂分别为A_______,C______,D______。
⑶若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将__________(填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中测定结果中NaHCO3的含量将___________;若撤去E装置,则测得Na2CO3·10H2O的含量__________。
⑷若样品质量为w g,反应后C、D增加的质量分别为m1 g、m2 g,由此可知混合物中
NaHCO3质量分数为_____________________(用含w、m1、m2的代数式表示)
⑴赶走装置中空气含有的水蒸气和二氧化碳,关闭b,打开a,缓缓通入空气,⑵碱石灰 无水CaCl2(或P2O5等) 碱石灰⑶偏低 无影响 偏低⑷21m2/11w
该题综合考查元素化合物性质,测定混合物中各成分的质量分数。解题时必须结合实验装置和物质的性质进行综合分析。将混合物加热,产生H2O(g)、CO2等气体,应在C、D中分别吸收,由干燥剂的性质知应先吸收水,再吸收二氧化碳,即C中的干燥剂吸水后不能吸收CO2。由D的增重(NaHCO3分解产生的CO2的质量)可求出NaHCO3质量。由C的增重(Na2CO3·10H2O分解产生的H2O及已经知道的NaHCO3分解产生的H2O的质量)可求出Na2CO3·10H2O的质量,从而求出NaCl的质量。故应在实验前想法赶出装置中的空气,关键操作应是赶B中的空气,所以关闭b,打开a就成为操作的关键,缓缓通入则是为了赶出效果更好。E中碱石灰可防止外界空气中的H2O(g)、CO2进入装置D影响实验效果。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 溶度积/25℃
溶度积/25℃
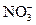 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是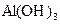
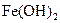 时,吸取NaOH溶液的胶头滴管的末端应插入
时,吸取NaOH溶液的胶头滴管的末端应插入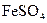 溶液中,再逐渐注入NaOH溶液
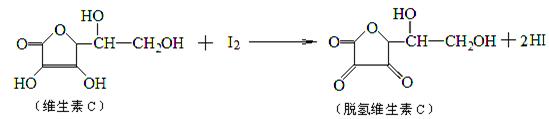
溶液中,再逐渐注入NaOH溶液 法测定某橙汁中维生素C的含量,其化学方程式如下所示.下列说法正确的是
法测定某橙汁中维生素C的含量,其化学方程式如下所示.下列说法正确的是