0 102267 102275 102281 102285 102291 102293 102297 102303 102305 102311 102317 102321 102323 102327 102333 102335 102341 102345 102347 102351 102353 102357 102359 102361 102362 102363 102365 102366 102367 102369 102371 102375 102377 102381 102383 102387 102393 102395 102401 102405 102407 102411 102417 102423 102425 102431 102435 102437 102443 102447 102453 102461 203614

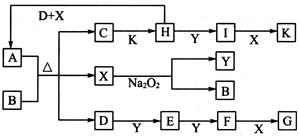
 学方程式是 。A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是 。
学方程式是 。A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是 。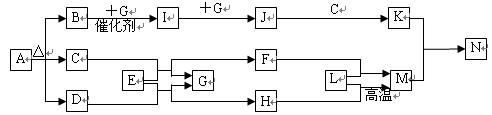
 : 。
: 。
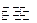 2I(g);
2I(g);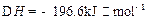 。当加入4 mol H和2 mol Y后,放出345 kJ的热量时,H的转化率最接近于__________(填字母)。
。当加入4 mol H和2 mol Y后,放出345 kJ的热量时,H的转化率最接近于__________(填字母)。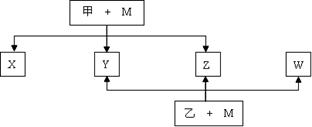

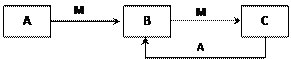
 6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)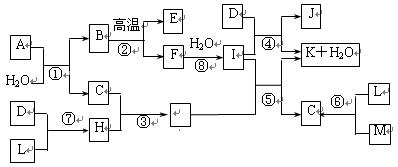
 两容积相等的密闭容器。
两容积相等的密闭容器。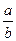 ________
________ 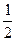 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。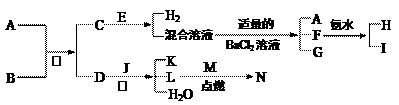 A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
 .
.