0 102204 102212 102218 102222 102228 102230 102234 102240 102242 102248 102254 102258 102260 102264 102270 102272 102278 102282 102284 102288 102290 102294 102296 102298 102299 102300 102302 102303 102304 102306 102308 102312 102314 102318 102320 102324 102330 102332 102338 102342 102344 102348 102354 102360 102362 102368 102372 102374 102380 102384 102390 102398 203614
 物的水化物之间的相互反应的化学方程式: 。
物的水化物之间的相互反应的化学方程式: 。 ,第________族;
,第________族; ) 写出铜与稀HBO3溶液反应的离子反应方程式
) 写出铜与稀HBO3溶液反应的离子反应方程式  种元素最高价氧化物的水化物的酸性最强的是 (填化学式),其中化学性质明显不同于其他三种化合物的
种元素最高价氧化物的水化物的酸性最强的是 (填化学式),其中化学性质明显不同于其他三种化合物的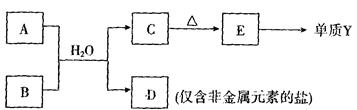
 是 。
是 。 的溶液作用下,可形成燃料电池,则该电池的负极反应式为 。
的溶液作用下,可形成燃料电池,则该电池的负极反应式为 。
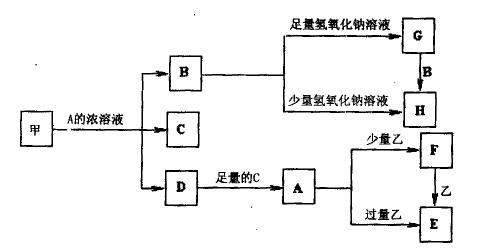
 关系如下图所示:则原F溶液的浓度为 mol/L。
关系如下图所示:则原F溶液的浓度为 mol/L。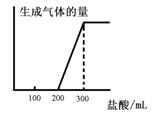
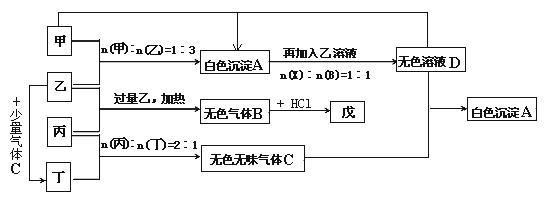
 气的水溶液充分反应可生成两种强酸,该反应的化学方程式
气的水溶液充分反应可生成两种强酸,该反应的化学方程式 写出其一级电离方程式: 。
写出其一级电离方程式: 。 已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为: 。
已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为: 。 2YX3(g)在一定条件下达到平衡。
2YX3(g)在一定条件下达到平衡。