题目内容
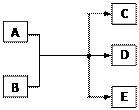
已知四种元素A、B、C、D 为1到20号元素,且原子序数依次增大,A的核外电子数与其电子层数相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。请回答下列问题:
(1) C在周期表中的位置第 ______周期 ,第________族;
,第________族;
(2 ) 写出铜与稀HBO3溶液反应的离子反应方程式
) 写出铜与稀HBO3溶液反应的离子反应方程式
(3) A、B形成的化合物的结构式____ ;其中含有的化学键类型为________,用电子式表示该化合物形成过程 ___ _。
(4)写出D与C形成化合物的电子式____ ____。
(1) C在周期表中的位置第 ______周期
 ,第________族;
,第________族;(2
 ) 写出铜与稀HBO3溶液反应的离子反应方程式
) 写出铜与稀HBO3溶液反应的离子反应方程式 (3) A、B形成的化合物的结构式____ ;其中含有的化学键类型为________,用电子式表示该化合物形成过程 ___ _。
(4)写出D与C形成化合物的电子式____ ____。
(方程式2分,其余每空1分,共8分)
(1)三(1分) ⅥA(1分,不写A者不给分)
(2)3Cu + 8H+ +2NO3-=" =" 3Cu2++ 2NO↑ + 4H2O
(2分,化学式有错者得0分,未配平者扣1分。不标气体符号的扣1分)
(3)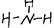 (1分)极性键(1分),有错别字者不给分)
(1分)极性键(1分),有错别字者不给分)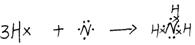 (1分)
(1分)
(4)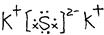 (1分)
(1分)
(1)三(1分) ⅥA(1分,不写A者不给分)
(2)3Cu + 8H+ +2NO3-=" =" 3Cu2++ 2NO↑ + 4H2O
(2分,化学式有错者得0分,未配平者扣1分。不标气体符号的扣1分)
(3)
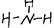 (1分)极性键(1分),有错别字者不给分)
(1分)极性键(1分),有错别字者不给分)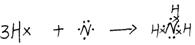 (1分)
(1分)(4)
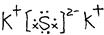 (1分)
(1分)略

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案
相关题目
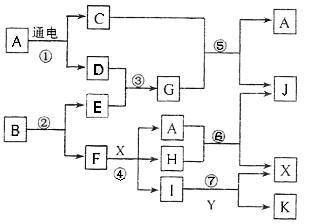
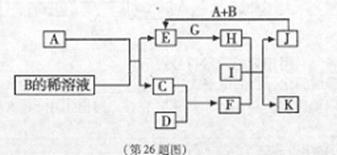
 请按要求填空:(1)写出A的电子式 、F元素在周期表位置 (2)反应⑤的化学方程式为: 。
请按要求填空:(1)写出A的电子式 、F元素在周期表位置 (2)反应⑤的化学方程式为: 。 ,该化合物与CA3和A2D的熔点由高到低的顺序为 (用化学式表示)。
,该化合物与CA3和A2D的熔点由高到低的顺序为 (用化学式表示)。 写出其一级电离方程式: 。
写出其一级电离方程式: 。 已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为: 。
已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为: 。 2YX3(g)在一定条件下达到平衡。
2YX3(g)在一定条件下达到平衡。