题目内容
5.下列离子方程式书写不正确的是( )| A. | 氯水和碘化钾反应:Cl2+2I-=2Cl-+I2 | |
| B. | 盐酸与AgNO3溶液反应:HCl+Ag+=H++Ag Cl↓ | |
| C. | 氢氧化钙溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O | |
| D. | 二氧化锰和盐酸制氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
分析 A.反应生成KCl和碘,遵循电子和电荷守恒;
B.反应生成AgCl和硝酸,盐酸为强酸;
C.反应生成氯化钠、次氯酸钠和水;
D.反应生成氯化锰、氯气和水.
解答 解:A.氯水和碘化钾反应的离子反应为Cl2+2I-=2Cl-+I2,故A正确;
B.盐酸与AgNO3溶液反应的离子反应为Cl-+Ag+=AgCl↓,故B错误;
C.氢氧化钙溶液吸收氯气的离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故C正确;
D.二氧化锰和盐酸制氯气的离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故D正确;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
18.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
(1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知反应N2(g)+3H2(g)?2NH3(g)△H=akJ•mol-1.试根据表中所列键能数据计算a的数值-93:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
已知:C(石墨,s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1①
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1②
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖斯定律,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ•mol-1.
16.下列应用中涉及氧化反应的是( )
| A. | 用明矾净化水 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| C. | 用装有硅胶的透气小袋防潮 | |
| D. | 屠呦呦用乙醚从中药中萃取青蒿素 |
13.a、b、c、d均为短周期元素,它们原子的最外层电子数分别为1、3、6、7.a、d的简单离子的电子层结构相同,b、c原子的次外层电子数均为8.下列说法正确的是( )
| A. | 单质的沸点:a>d>c | |
| B. | 简单离子的半径:c>d>a>b | |
| C. | a、b、c简单离子都会破坏水的电离平衡 | |
| D. | a、b、d的最高价氧化物对应的水化合物两两皆能反应 |
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 22.4L O2的分子数约为NA | |
| B. | 标准状况下,11.2L H2O的分子数约为0.5NA | |
| C. | 1 L 1mol/L的NaOH溶液中Na+的数目为NA | |
| D. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1NA |
17.下列各组顺序的排列不正确的是( )
| A. | 熔点:金刚石>干冰 | B. | 稳定性:SiH4>H2S | ||
| C. | 碱性:KOH>Al(OH)3 | D. | 离子半径:O2->Na+ |
14.废弃物资源化对于建设资源节约型社会具有重要的意义.研究小组测某矿灰的成分,其主要成分为Fe,可能还含有KCl、FeO、Fe2O3、MgO、SiO2、MnO2中的若干种.为了确认其成分,某同学依次进行了以下实验:
①将过量的稀盐酸加入矿灰中,充分反应后过滤得到溶液甲和固体乙
②取少量溶液甲滴加AgNO3溶液,生成白色沉淀
③取少量溶液甲分成两等份,向其中一份滴加酸性高锰酸钾溶液,高锰酸钾溶液褪色;向另一份滴加KSCN溶液,溶液变成血红色
④取少量溶液甲加入过量NaOH溶液,并置于空气中.充分反应后经过滤、洗涤、灼烧得到1.60g固体丙,将固体丙置于氢气流中加热充分反应后得到1.12g固体丁
根据以上实验现象或数据,该同学得出的结论正确的是( )
①将过量的稀盐酸加入矿灰中,充分反应后过滤得到溶液甲和固体乙
②取少量溶液甲滴加AgNO3溶液,生成白色沉淀
③取少量溶液甲分成两等份,向其中一份滴加酸性高锰酸钾溶液,高锰酸钾溶液褪色;向另一份滴加KSCN溶液,溶液变成血红色
④取少量溶液甲加入过量NaOH溶液,并置于空气中.充分反应后经过滤、洗涤、灼烧得到1.60g固体丙,将固体丙置于氢气流中加热充分反应后得到1.12g固体丁
根据以上实验现象或数据,该同学得出的结论正确的是( )
| A. | 根据①可推出矿灰中一定含有SiO2 | |
| B. | 根据②可推出矿灰中一定含有KCl | |
| C. | 根据③可推出矿灰中一定含有FeO和Fe2O3 | |
| D. | 根据④可推出固体丙中一定不含MgO |
15.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 用铜为电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 金属铝的冶炼:2AlCl3(熔融)$\frac{\underline{\;通电\;}}{\;}$2Al+3Cl2↑ | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 碱性氢氧燃料电池的正极反应为:O2+4e-+2H2O═4OH- |

 $→_{Zn/H_{2}O}^{O_{3}}$
$→_{Zn/H_{2}O}^{O_{3}}$ +
+
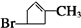 、E
、E .
.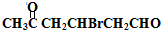 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$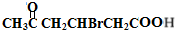 +Cu2O↓+2H2O.
+Cu2O↓+2H2O. .
.