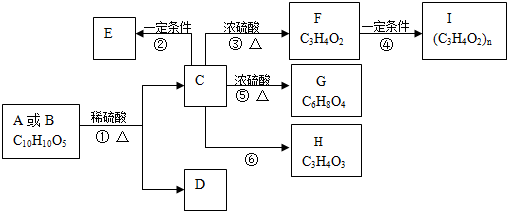
题目内容
用CuFeS2冶炼钢的反应为8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2.若CuFeS2中Fe的化合价为+2价,下列关于该反应的说法正确的是( )
| ||
| A、CuFeS2只作还原剂 |
| B、Fe元素全部被氧化 |
| C、还原产物是Cu、FeO、Fe2O3和SO2 |
| D、若生成1molCu,则反应中转移2mol电子 |
考点:氧化还原反应
专题:
分析:由8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2反应可知Cu元素化合价由+2价降低到0价,Fe元素的化合价由+2价升高为+3价,S元素的化合价由-2价升高为+4价,O元素的化合价由0降低为-2价,以此来解答.
| ||
解答:
解:A.反应中Cu元素化合价降低,S元素化合价升高,则CuFeS2既是氧化剂也是还原剂,故A错误;
B.反应生成FeO、Fe2O3,可知部分Fe被氧化,故B错误;
C.反应中Cu、O元素化合价降低,则还原产物是Cu、FeO、Fe2O3和SO2,故C正确;
D.反应中Cu、O元素化合价降低,由方程式可知当生成8molCu时得到电子的物质的量为8mol×(2-0)+21mol×4=100mol,则若生成1molCu,则反应中转移
=12.5mol电子,故D错误.
故选C.
B.反应生成FeO、Fe2O3,可知部分Fe被氧化,故B错误;
C.反应中Cu、O元素化合价降低,则还原产物是Cu、FeO、Fe2O3和SO2,故C正确;
D.反应中Cu、O元素化合价降低,由方程式可知当生成8molCu时得到电子的物质的量为8mol×(2-0)+21mol×4=100mol,则若生成1molCu,则反应中转移
| 100 |
| 8 |
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子的考查,选项C为易错点,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
下列对Na2CO3与NaHCO3的描述正确的是( )
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
在给定的四种溶液中,含有以下各种微粒,一定能大量共存的是( )
| A、饱和Na2CO3溶液中:NH4+、C6H5OH、NO3-、NH3?H2O |
| B、常温下葡萄糖溶液中:SCN-、Cl-、K+、NH4+ |
| C、溴水中:Na+、CO32-、NH4+、SO42- |
| D、pH大于7的溶液:Na+、Ba2+、SO32-、ClO- |
设NA为阿佛加德罗常数,下列叙述中不正确的是( )
| A、常温下,46 g 红棕色二氧化氮气体中含有N、O原子个数和为3NA |
| B、标准状况下,1 NA CH3Cl所占的体积约为22.4 L |
| C、N2(g)+3H2(g)?2NH3(g)△H=-a kJ/mol,现向一密闭容器中通入2 NA个氨气分子反应完全后,吸收a kJ热量 |
| D、足量铜与1 L 18mol?L-1浓硫酸反应可以得到SO2的分子总数小于9 NA |
下表是元素周期表一部分.X、Y、Z均为短周期元素,X、Z的质子数之和为23,下列说法正确的是( )
| X | |||
| Y | Z | ||
| W |
| A、W的原子序数比Z的大9 |
| B、Y的最高价氧化物溶于水,与水反应得到酸 |
| C、W的单质能与Z的一种氧化物的水溶液反应生成两种强酸 |
| D、Z的单质在一定条件下可与铁粉反应,将铁粉氧化为+3价 |
根据原子结构及元素周期律的知识,下列推断正确的是( )
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B、核外电子排布相同的微粒化学性质相同 |
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D、还原性强弱:F-<Cl-<I- |
下列离子检验方法正确的是( )
| A、某溶液中加入AgNO3溶液,生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液中加入BaCl2溶液,生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液中加入稀硫酸,生成无色气体,说明原溶液中有CO32- |
| D、某溶液中加入NaOH溶液,生成能使湿红色石蕊试纸变蓝的气体,说明原溶液中有NH4+ |
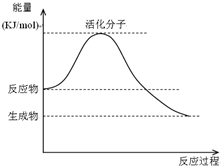 (1)如图是某化学反应中的能量变化图.
(1)如图是某化学反应中的能量变化图.