题目内容
下列对Na2CO3与NaHCO3的描述正确的是( )
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
考点:钠的重要化合物
专题:
分析:A.Na2CO3比NaHCO3易溶于水;
B.NaHCO3不稳定,加热易分解;
C.碳酸钠和碳酸氢钠都能和澄清石灰水反应生成碳酸钙沉淀;
D.碳酸根离子的水解程度大于碳酸氢根离子.
B.NaHCO3不稳定,加热易分解;
C.碳酸钠和碳酸氢钠都能和澄清石灰水反应生成碳酸钙沉淀;
D.碳酸根离子的水解程度大于碳酸氢根离子.
解答:
解:A.在饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,说明Na2CO3比NaHCO3易溶于水,故A正确;
B.NaHCO3不稳定,加热易分解:2NaHCO3
Na2CO3+CO2↑+H2O,碳酸钠受热不易分解,较稳定,故B错误;
C.加热时碳酸钠和碳酸氢钠分别和氢氧化钙反应的方程式如下:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH,所以都能发生复分解反应,故C错误;
D.碳酸根离子的水解程度大于碳酸氢根离子,且CO32-以第一步水解为主,则等浓度的溶液,Na2CO3溶液的碱性较强,故D错误;
故选A.
B.NaHCO3不稳定,加热易分解:2NaHCO3
| ||
C.加热时碳酸钠和碳酸氢钠分别和氢氧化钙反应的方程式如下:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH,所以都能发生复分解反应,故C错误;
D.碳酸根离子的水解程度大于碳酸氢根离子,且CO32-以第一步水解为主,则等浓度的溶液,Na2CO3溶液的碱性较强,故D错误;
故选A.
点评:本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
使H2SO4与过量Zn反应速率下降但不影响H2 的量,应加入( )
| A、Na2CO3 (s) |
| B、(NH4)2SO4 (s) |
| C、K2SO4 (aq) |
| D、H2O (l) |
| E、CH3COONa(s) |
下列说法不正确的是( )
| A、依据丁达尔现象可区分氯化钠溶液和蛋白质溶液 |
| B、仅由同一种元素组成的物质一定是纯净物 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、Na2O2能与CO2反应产生O2,可用作高空飞行或潜水的供氧剂 |
将Al片投入某无色澄清溶液中,产生大量H2,则该溶液中可能含有的微粒是( )
| A、K+、OH-、NO3-、Cl- |
| B、H+、Na+、CO32-、Cl- |
| C、H+、K+、NO3-、Cl- |
| D、Cu2+、H+、Cl-、SO42- |
用CuFeS2冶炼钢的反应为8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2.若CuFeS2中Fe的化合价为+2价,下列关于该反应的说法正确的是( )
| ||
| A、CuFeS2只作还原剂 |
| B、Fe元素全部被氧化 |
| C、还原产物是Cu、FeO、Fe2O3和SO2 |
| D、若生成1molCu,则反应中转移2mol电子 |
下列叙述错误的是( )
| A、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| B、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
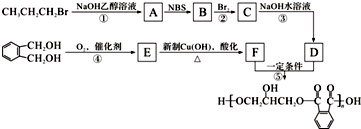
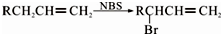 .
.
 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有