题目内容
从环己烷可制备1,4-环己二醇的二醋酸酯.下面是有关的8步反应(其中所有无机产物都已略去):
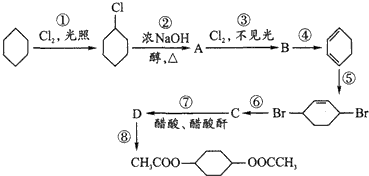
其中有3步属于取代反应、2步属于消去反应、3步属于加成反应.
反应①、 和 属于取代反应.
化合物的结构简式是:B 、C .
反应④所用试剂和条件是 .

其中有3步属于取代反应、2步属于消去反应、3步属于加成反应.
反应①、
化合物的结构简式是:B
反应④所用试剂和条件是
考点:有机物的合成,取代反应与加成反应
专题:有机化合物的获得与应用
分析: 在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 .
.
 在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 .
.解答:
解: 在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 .
.
故①为取代反应,②为消去反应,③为加成反应,④为消去反应,⑤为加成反应,⑥为取代反应,⑦为取代反应;
B的结构简式为: ;C的结构简式为:
;C的结构简式为: ;
;
 发生消去反应生成
发生消去反应生成 的反应条件是浓氢氧化钠、醇、加热;
的反应条件是浓氢氧化钠、醇、加热;
故答案为:⑥;⑦; ;
; ;浓氢氧化钠、醇、加热.
;浓氢氧化钠、醇、加热.
 在氢氧化钠醇作用下发生消去反应生成A,A为
在氢氧化钠醇作用下发生消去反应生成A,A为 ,
, 与氯气发生加成反应生成B,B为
与氯气发生加成反应生成B,B为 ,
, 发生消去反应生成
发生消去反应生成 ,
, 与溴水发1,4加成生成
与溴水发1,4加成生成 ,
, 发生水解生成C,C为
发生水解生成C,C为 ,
, 与醋酸酐发生酯化反应生成D,D为
与醋酸酐发生酯化反应生成D,D为 ,
, 与氢气发生加成反应生成
与氢气发生加成反应生成 .
.故①为取代反应,②为消去反应,③为加成反应,④为消去反应,⑤为加成反应,⑥为取代反应,⑦为取代反应;
B的结构简式为:
 ;C的结构简式为:
;C的结构简式为: ;
; 发生消去反应生成
发生消去反应生成 的反应条件是浓氢氧化钠、醇、加热;
的反应条件是浓氢氧化钠、醇、加热;故答案为:⑥;⑦;
 ;
; ;浓氢氧化钠、醇、加热.
;浓氢氧化钠、醇、加热.
点评:本题重点考查反应条件与反应类型的关系,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
萃取碘水中的碘,可用的萃取剂是( )
①酒精 ②汽油 ③四氯化碳.
①酒精 ②汽油 ③四氯化碳.
| A、只有③ | B、②③ |
| C、①③ | D、①②③ |

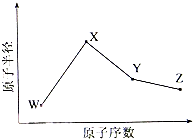 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大.