题目内容
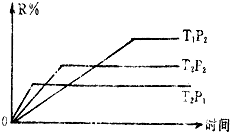 在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )
在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )| A、正反应为吸热反应 L是气体 |
| B、正反应为放热反应 L是气体 |
| C、正反应为吸热反应 L是固体 |
| D、正反应为放热反应 L是固体或液体 |
考点:体积百分含量随温度、压强变化曲线
专题:
分析:由图象可知,温度为T2时,根据到达平衡的时间可知P2>P1,且压强越大,R的含量越高,说明平衡正向移动,正反应为气体体积减小的反应;
压强为P2时,根据到达平衡的时间可知T2>T1,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应.
压强为P2时,根据到达平衡的时间可知T2>T1,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应.
解答:
解:由图象可知,温度为T2时,根据到达平衡的时间可知P2>P1,且压强越大,R的含量越高,说明平衡正向移动,正反应为气体体积减小的反应,故L为固体或液体;
压强为P2时,根据到达平衡的时间可知T2>T1,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应;
A.由上述分析可知,正反应放热,L是固体或液体,故A错误;
B.由上述分析可知,正反应放热,L是固体或液体,故B错误;
C.由上述分析可知,正反应放热,L是固体或液体,故C错误;
D、由上述分析可知,正反应放热,L是固体或液体,故D正确,
故选D.
压强为P2时,根据到达平衡的时间可知T2>T1,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应;
A.由上述分析可知,正反应放热,L是固体或液体,故A错误;
B.由上述分析可知,正反应放热,L是固体或液体,故B错误;
C.由上述分析可知,正反应放热,L是固体或液体,故C错误;
D、由上述分析可知,正反应放热,L是固体或液体,故D正确,
故选D.
点评:本题考查化学平衡图象问题,难度不大,本题注意根据图象判断问题、压强的大小,根据温度、压强对平衡移动的影响分析.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
某水溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-中的若干种离子.某同学取100m L的溶液分成两等份进行如下实验:
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲.
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体.
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到 11.65g固体.
下列结论正确的是( )
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲.
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体.
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到 11.65g固体.
下列结论正确的是( )
| A、实验①中产生的气体为氨气,并可得原溶液中c (NH4+)=0.2 mol?L-1 |
| B、实验③中的白色沉淀中一定有BaSO4,无BaCO3 |
| C、原溶液中一定有K+,且c (K+)=0.5 mol?L-1 |
| D、若要判断原溶液中是否有Cl-,无需另外设计实验验证 |
化学与生活、社会密切相关.下列说法错误的是( )
| A、亚硝酸盐属丁食物防腐剂,可以适量地添加于食物中 |
| B、氨气泄漏时,可喷洒大量的水以减少氨气的扩散 |
| C、漂白粉在空气中不稳定,可用于漂白纸张 |
| D、大量燃烧化石燃料是造成雾霾大气的重要原因 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、由强酸与强碱等物质的量反应得到的溶液 |
| C、使酚酞试液呈无色的溶液 |
| D、c(H+)=c(OH-)=10-6mol/L的溶液 |
 一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示下列描述正确的是( )
一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示下列描述正确的是( )| A、反应开始到10 s,用Z表示的反应速率为0.158 mol/(L?s) |
| B、反应开始到10 s,X的物质的量浓度减少了0.79 mol/L |
| C、反应开始到10 s时,Y的转化率为79% |
| D、反应的化学方程式为:X(g)+Y(g)?Z(g) |
下列各组分子中都属于含极性键的非极性分子的是( )
| A、CO2、H2S |
| B、C2H4、CH4 |
| C、Cl2、C2H2 |
| D、NH3、HCl |
下列分子式表示的物质,具有同分异构体的是( )
| A、C3H6 |
| B、C3H8 |
| C、CH2Cl2 |
| D、C2H4 |
下列物质中属于非电解质的是( )
| A、乙醇 |
| B、O2 |
| C、Na2CO3 |
| D、NaOH |