题目内容
化学与生活、社会密切相关.下列说法错误的是( )
| A、亚硝酸盐属丁食物防腐剂,可以适量地添加于食物中 |
| B、氨气泄漏时,可喷洒大量的水以减少氨气的扩散 |
| C、漂白粉在空气中不稳定,可用于漂白纸张 |
| D、大量燃烧化石燃料是造成雾霾大气的重要原因 |
考点:常见的食品添加剂的组成、性质和作用,氨的化学性质,常见的生活环境的污染及治理
专题:
分析:A.根据食品保存的基本原理采用一定的方法杀死或抑制微生物在食品中的生长、繁殖分析探讨;
B.氨气有毒,氨气极易溶于水,可以使用水吸收氨气;
C.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性;
D.大量燃烧化石燃料可产生有害气体和烟尘.
B.氨气有毒,氨气极易溶于水,可以使用水吸收氨气;
C.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性;
D.大量燃烧化石燃料可产生有害气体和烟尘.
解答:
解:A.根据食物腐败变质的原因,食品保存就要尽量的杀死或抑制微生物的生长和大量繁殖,可以避免食物的腐败变质,亚硝酸盐具有防腐性,可与肉品中的肌红素结合而更稳定,所以常在食品加工业被添加在香肠和腊肉中作为保色剂,以维持良好外观;其次,它可以防止肉毒梭状芽孢杆菌的产生,提高食用肉制品的安全性,所以可以适量地添加于食物中,故A正确;
B.氨气极易溶于水,所以氨气泄漏时可喷洒大量水进行处理,故B正确;
C.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性,表现性质不同,故C错误;
D.大量燃烧化石燃料可产生有害气体和烟尘,是造成雾霾天气的一种重要因素,故D正确.
故选C.
B.氨气极易溶于水,所以氨气泄漏时可喷洒大量水进行处理,故B正确;
C.漂白粉在空气中与水、二氧化碳反应生成不稳定的次氯酸,用于漂白纸张为漂白性,表现性质不同,故C错误;
D.大量燃烧化石燃料可产生有害气体和烟尘,是造成雾霾天气的一种重要因素,故D正确.
故选C.
点评:本题考查较为综合,涉及防腐剂、漂白粉、氨气以及环境污染等问题,为高考常见题型,侧重于学生的双基的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各项叙述中,类比推理正确的是( )
| A、铜丝在氧气中燃烧生成是CuO,则铁丝在氧气中燃烧生成Fe2O3 |
| B、少量CO2通入NaOH溶液中生成Na2CO3,则少量CO2通入C6H5ONa溶液中也生成Na2CO3 |
| C、甲醛能发生银镜反应,则甲酸甲酯也能发生银镜反应 |
| D、金刚石的硬度大,则C60的硬度也大 |
遇到下列情况,处理恰当的是( )
| A、不小心将少量浓硫酸沾到皮肤,立即用水冲洗 |
| B、皮肤上沾有浓碱溶液时,立即用酒精冲洗 |
| C、为了避免浪费,应该把实验用剩的药品放回原试剂瓶中 |
| D、连接并组装成套仪器时,一般按自下而上、从左到右的顺序进行安装 |
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | ||
| B、0.1mol/LH2SO4与0.1mol/L氨水等体积混合:c(H+)>c(NH4+)>c(SO42-)>c(OH-) | ||
C、0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:
| ||
| D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
家用消毒液的发生器是以精盐和自来水为反应物,通电时,发生器的电解槽的极板上产生大量气泡,切断电源后,生成液具有强烈的杀菌消毒能力.与该反应器工作原理直接有关的化学方程式是( )
| A、2NaOH+Cl2═NaCl+NaClO+H2O |
| B、H2+Cl2═2HCl |
| C、2NaCl(熔融)=2Na+Cl2↑ |
| D、2HClO═2HCl+O2↑ |
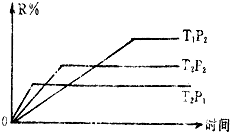 在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )
在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )| A、正反应为吸热反应 L是气体 |
| B、正反应为放热反应 L是气体 |
| C、正反应为吸热反应 L是固体 |
| D、正反应为放热反应 L是固体或液体 |
在强酸性溶液中下列离子能大量共存的是( )
| A、Ca2+、Na+、OH-、CO32- |
| B、Ag+、SO42-、HCO3-、Cl- |
| C、Cu2+、Na+、SO42-、NO3- |
| D、NH4+、S2-、Mg2+、Cu2+ |