题目内容
根据化学方程式:2N2O
2N2+O2,反应起始时:c(O2)、c(N2)皆为0,c(N2O)=c mol?L-1,t min后c(O2)=a mol?L-1,求:
(1)t min时c(N2)为 ;
(2)t min时c(N2O)为 ;
(3)t min内O2平均反应速率为 .
| △ |
(1)t min时c(N2)为
(2)t min时c(N2O)为
(3)t min内O2平均反应速率为
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:(1)根据参加反应的物质的物质的量之比等于化学计量数之比进行计算;
(2)根据参加反应的物质的物质的量之比等于化学计量数之比进行计算;
(3)根据v=
进行计算.
(2)根据参加反应的物质的物质的量之比等于化学计量数之比进行计算;
(3)根据v=
| △c |
| t |
解答:
解(1)2N2O
2N2+O2,t min后c(O2)=a mol?L-1,则t min时c(N2)为2×a mol?L-1=2a mol?L-1,
故答案为:2a mol?L-1;
(2)t min后c(O2)=a mol?L-1,则t min时参加反应的c(N2O)为2×a mol?L-1=2a mol?L-1,故t min时c(N2O)为c mol?L-1-2a mol?L-1=(c-2a)mol?L-1,
故答案为:(c-2a)mol?L-1;
(3)t min内O2平均反应速率为
=
mol?L-1?min-1,故答案为:
mol?L-1?min-1.
| △ |
故答案为:2a mol?L-1;
(2)t min后c(O2)=a mol?L-1,则t min时参加反应的c(N2O)为2×a mol?L-1=2a mol?L-1,故t min时c(N2O)为c mol?L-1-2a mol?L-1=(c-2a)mol?L-1,
故答案为:(c-2a)mol?L-1;
(3)t min内O2平均反应速率为
| amol?L-1 |
| tmin |
| a |
| t |
| a |
| t |
点评:本题考查化学反应速率及物质的量浓度的相关计算,难度不大.把握参加反应的物质的物质的量之比等于化学计量数之比为解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
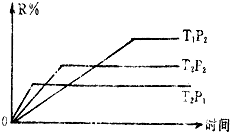 在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )
在密闭容器中进行下列反应:M(g)+N(g)═R(g)+2L.此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是( )| A、正反应为吸热反应 L是气体 |
| B、正反应为放热反应 L是气体 |
| C、正反应为吸热反应 L是固体 |
| D、正反应为放热反应 L是固体或液体 |
将BaO2放入密闭真空容器中,反应BaO2(s)?BaO(s)+
O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| 1 |
| 2 |
| A、氧气压强不变 | ||||
| B、BaO质量增加 | ||||
| C、BaO2质量不变 | ||||
D、平衡常数K=
|
下列分子或离子在指定条件的分散系中能大量共存的是( )
| A、Ca(NO3)2溶液中:Fe2+、H+、Cl-、SO42- |
| B、使pH试纸变蓝的溶液中:K+、NH4+、S-、SO32- |
| C、水电离出的c(H+)=10-12 mol?L-1的溶液中:Na+、Ba2+、HCO3-、CH3COO- |
| D、透明的强酸性溶液中:Al3+、Fe3+、Cl-、SO42 |
在强酸性溶液中下列离子能大量共存的是( )
| A、Ca2+、Na+、OH-、CO32- |
| B、Ag+、SO42-、HCO3-、Cl- |
| C、Cu2+、Na+、SO42-、NO3- |
| D、NH4+、S2-、Mg2+、Cu2+ |
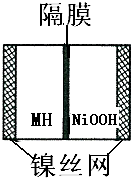 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )| A、放电时正极反应为:NiOOH+H2O+e-═Ni(OH)2+OH- |
| B、电池的电解液可为稀H2SO4溶液 |
| C、充电时负极反应为:MH+OH--e-═H2O+M |
| D、MH是一类储氢材料,其所含氢密度越大,电池的能量密度越高 |