题目内容
 某课外小组的同学收集了含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,他们在实验室按如图所示装置进行实验〔气体通过装置A速度很慢,假设在此处发生的反应完全;碱石灰(CaO和NaOH的混合物)过量〕.
某课外小组的同学收集了含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,他们在实验室按如图所示装置进行实验〔气体通过装置A速度很慢,假设在此处发生的反应完全;碱石灰(CaO和NaOH的混合物)过量〕.(1)A中碱石灰的作用是
(2)B中发生反应的化学方程式是
(3)该实验能证明混合气体中存在CO的现象是
(4)若反应前称得硬质玻璃管内的氧化铁质量为10g,反应一段时间后冷却再次称量发现硬质玻璃管内的固体质量变为7.6g,则反应了的氧化铁的质量分数为
考点:探究物质的组成或测量物质的含量,实验装置综合
专题:实验设计题
分析:含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,由实验装置可知,碱石灰干燥气体,吸收水蒸气、二氧化碳,B中发生CO与氧化铁的反应,C中石灰水变浑浊,说明生成二氧化碳,则原混合气体含CO,D为尾气处理,以此来解答.
解答:
解:含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,由实验装置可知,碱石灰干燥气体,吸收水蒸气、二氧化碳,B中发生CO与氧化铁的反应,C中石灰水变浑浊,说明生成二氧化碳,则原混合气体含CO,D为尾气处理,
(1)A中碱石灰的作用是除去废气中的水蒸气和二氧化碳气体,故答案为:除去废气中的水蒸气和二氧化碳气体;
(2)B中发生反应的化学方程式是3CO+Fe2O3
2Fe+3CO2,故答案为:3CO+Fe2O3
2Fe+3CO2;
(3)能证明混合气体中存在CO的现象是C中红色变黑色,D中石灰水变浑浊,故答案为:C中红色变黑色,D中石灰水变浑浊;
(4)由反应可知,固体减少质量为10g-7.6g=2.4g,则设反应了的氧化铁的质量为x,
3CO+Fe2O3
2Fe+3CO2,质量差
160 112 48
x 2.4g
=
,解得x=8g,
所以反应了的氧化铁的质量分数为
×100%=80%,故答案为:80%.
(1)A中碱石灰的作用是除去废气中的水蒸气和二氧化碳气体,故答案为:除去废气中的水蒸气和二氧化碳气体;
(2)B中发生反应的化学方程式是3CO+Fe2O3
| ||
| ||
(3)能证明混合气体中存在CO的现象是C中红色变黑色,D中石灰水变浑浊,故答案为:C中红色变黑色,D中石灰水变浑浊;
(4)由反应可知,固体减少质量为10g-7.6g=2.4g,则设反应了的氧化铁的质量为x,
3CO+Fe2O3
| ||
160 112 48
x 2.4g
| 160 |
| x |
| 48 |
| 2.4g |
所以反应了的氧化铁的质量分数为
| 8g |
| 10g |
点评:本题考查物质组成实验方案的设计,为高频考点,把握装置的作用及差量法计算为解答的关键,侧重分析、计算与实验能力的考查,题目难度中等.

练习册系列答案
相关题目
下列图示操作中,不正确的是( )
A、 过滤 |
B、 蒸发食盐水 |
C、 萃取时,振荡分液漏斗 |
D、 配制溶液时,将容量瓶反复上下颠倒,摇匀 |
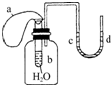 如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将观察到的现象是( )
如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将观察到的现象是( )| A、试管内水变为红色 |
| B、试管内有沉淀生成 |
| C、气球a被吹大 |
| D、U形管水位d高于c |
进行焰色反应检验K+时,有以下步骤,其中正确的操作顺序是( )
①蘸取待测液 ②置于酒精灯火焰上灼烧 ③透过蓝色钴玻璃观察 ④用稀盐酸洗净铂丝.
①蘸取待测液 ②置于酒精灯火焰上灼烧 ③透过蓝色钴玻璃观察 ④用稀盐酸洗净铂丝.
| A、④②①②③ | B、①②③④ |
| C、④①②③ | D、②①③④ |
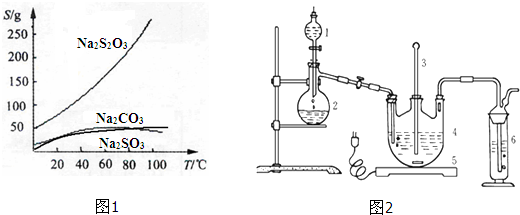


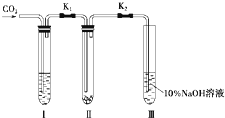 为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如图的实验装置,分别进行了甲、乙两次实验:
为了探究“二氧化碳是否在水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如图的实验装置,分别进行了甲、乙两次实验:
