题目内容
16.下列说法正确的是( )| A. | 蒸发时,应将蒸发皿中的溶液全部加热蒸干后停止加热 | |
| B. | 蒸馏实验开始时先通入冷凝水,再点燃酒精灯加热 | |
| C. | 萃取时,应选择有机萃取剂,且萃取剂的密度必须比水的密度小 | |
| D. | 分液时,分液漏斗中下层液体从下口放出,上层液体也从下口流出 |
分析 A.蒸发时,注意温度不能过高,防止固体迸溅;
B.为防止冷凝管破裂,应先接通冷凝水;
C.萃取剂的选择与密度无关;
D.分液时,应避免液体重新混合而污染.
解答 解:A.蒸发时,注意温度不能过高,防止溶固体迸溅,当有大量固体析出时,停止加热,用余热蒸干,故A错误;
B.实验开始时,为防止冷凝管破裂,应先接通冷凝水,再点燃酒精灯加热蒸馏烧瓶,故B正确;
C.萃取剂的密度不一定比水大,只要符合萃取剂与原溶剂互不相溶,溶质在萃取剂中的溶解度比在水中大,且萃取剂与水的密度有差别即可,故C错误;
D.分液时,下层液体从下口流出,上层液体从上口倒出,避免液体重新混合而污染,故D错误.
故选B.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验操作的可行性的评价以及注意事项,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列3个反应:
①S(s)+O2(g)→SO2(g)
②H2(g)+O2(g)→H2O2(l)
③C(s)+H2O(g)→CO(g)+H2(g)
按△S增加的顺序为( )
①S(s)+O2(g)→SO2(g)
②H2(g)+O2(g)→H2O2(l)
③C(s)+H2O(g)→CO(g)+H2(g)
按△S增加的顺序为( )
| A. | ②①③ | B. | ③②① | C. | ②③① | D. | ①③② |
7.在喷泉实验的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹子,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是( )
| a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | 4mol/L NaOH溶液 |
| C | Cl2 | 饱和NaCl溶液 |
| D | NO | 水 |
| A. | A | B. | B | C. | C | D. | D |
11. MCl晶体具有立方体结构,其晶胞结构如图所示,在该晶体中,每个M+周围与它最接近的且距离相等的M+的个数共有( )
MCl晶体具有立方体结构,其晶胞结构如图所示,在该晶体中,每个M+周围与它最接近的且距离相等的M+的个数共有( )
 MCl晶体具有立方体结构,其晶胞结构如图所示,在该晶体中,每个M+周围与它最接近的且距离相等的M+的个数共有( )
MCl晶体具有立方体结构,其晶胞结构如图所示,在该晶体中,每个M+周围与它最接近的且距离相等的M+的个数共有( )| A. | 6个 | B. | 8个 | C. | 12个 | D. | 16个 |
6.实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示.下列分析正确的是( )
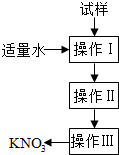

| A. | 操作Ⅰ是过滤,将固体分离除去 | |
| B. | 操作Ⅱ是加热浓缩.趁热过滤,除去杂质氯化钠 | |
| C. | 操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 | |
| D. | 操作Ⅰ~Ⅲ总共需两次过滤 |
 (或
(或 ).
).