题目内容
10.在无色透明溶液中,下列各组离子能大量共存的是( )| A. | Cu2+、K+、Cl-、NO3- | B. | Ag+、Na+、NO3-、Cl- | ||
| C. | Zn2+、Al3+、SO42-、Cl- | D. | Ba2+、NH4+、Cl-、CO32- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子可大量共存,并结合离子的颜色来解答.
解答 解:A.Cu2+为蓝色,与无色不符,故A不选;
B.Ag+、Cl-结合生成沉淀,不能共存,故B不选;
C.该组离子之间不反应,可大量共存,且离子均为无色,故C选;
D.Ba2+、CO32-结合生成沉淀,不能共存,故D不选;
故选C.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列实验不能达到实验目的或者实验操作不正确的是( )
| A. | 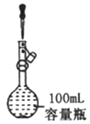 定容 | |
| B. | 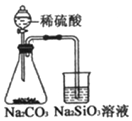 比较硫、碳、硅三种元素的非金属性强弱 | |
| C. | 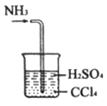 处理尾气 | |
| D. | 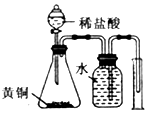 测定黄铜(Cu、Zn合金)中Zn的含量 |
1.在一密闭容器中有一氧化碳、甲醛、氢气、氧气的混合气体共23.6g,加入足量Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加10.8g,则原混合气体中氧气的物质的量是( )
| A. | 0.4 mol | B. | 0.34 mol | C. | 0.8 mol | D. | 0.74 mol |
18.下列关于元素及其化合物的说法不正确的是( )
| A. | Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应 | |
| B. | Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解 | |
| D. | 金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱 |
5.在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )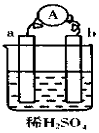

| A. | 碳棒上有气体放出,溶液pH变大 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,外电路中,电流从b极到a极 | |
| D. | a极上发生了氧化反应 |
15.下列与生活有关的实验设计不合理的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 用米汤检验含碘食盐中的KIO3 | ||
| C. | 用食醋除去热水壶中的水垢 | D. | 用NaOH溶液鉴别地沟油和矿物油 |
19.19世纪末,开始揭开原子内部的秘密,最早发现电子的科学家是( )
| A. | 英国的道尔顿 | B. | 英国的卢瑟福 | C. | 丹麦的玻尔 | D. | 英国的汤姆生 |
20.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气体 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 元素B的单质可被热的浓硫酸或浓硝酸氧化 | |
| D. | 化合物AE与CE含有相同类型的化学键 |