题目内容
15.将①H2S、②HCl、③CH4、④Ar、⑤NH3、⑥H2O、⑦MgO、⑧SiO2、⑨CO2、⑩NaCl、⑪NaOH、⑫NaHCO3等物质用序号按以下要求填空:(1)微粒间只存在共价键的是①②③⑤⑥⑧⑨,只存在离子键的是⑦⑩,既存在离子键,又存在共价键的是⑪⑫.
(2)属于离子化合物的是⑦⑩⑪⑫,其中只有离子键的化合物的电子式为
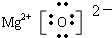 ;
; .
.(3)含共价键的分子是①②③⑤⑥⑨,属于共价化合物的是①②③⑤⑥⑧⑨.
分析 (1)非金属元素之间易形成共价键,非金属多原子分子、有机物、部分非金属氧化物等都含有共价键,活泼金属和活泼非金属元素之间易形成离子键,第IA族(H元素除外)、第IIA族和第VIA族、第VIIA族元素之间易形成离子键,由非金属氮原子、氢原子构成的铵根离子形成的化合物属于离子化合物,含离子键、共价键;
(2)含有离子键的化合物为离子化合物,离子化合物,其电子式 由阴、阳离子的电子式组合而成,相同的离子不能合并;
(3)分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体,离子化合物中可能含有共价键,只含共价键的化合物为共价键化合物.
解答 解:(1)①H2S只含有H-S共价键,②HCl只含有H-Cl共价键,③CH4只含有C-H共价键,④Ar不含共价键,⑤NH3只含有N-H共价键,⑥H2O只含有H-O共价键,⑦MgO只存在镁离子与氧离子之间的离子键,、⑧SiO2只含有Si-O共价键,⑨CO2只含有C=O共价键,⑩NaCl只存在钠离子与氯离子之间的离子键,⑪NaOH中钠离子与氢氧根离子之间存在离子键,氢原子与氧原子之间存在共价键,⑫NaHCO3中钠离子与碳酸氢根离子之间存在离子键,碳原子与氢原子、氧原子之间存在共价键,
故答案为:①②③⑤⑥⑧⑨;⑦⑩;⑪⑫;
(2)⑦MgO只存在镁离子与氧离子之间的离子键,属于离子化合物,⑩NaCl只存在钠离子与氯离子之间的离子键,属于离子化合物,⑪NaOH中钠离子与氢氧根离子之间存在离子键,氢原子与氧原子之间存在共价键,属于离子化合物,⑫NaHCO3中钠离子与碳酸氢根离子之间存在离子键,碳原子与氢原子、氧原子之间存在共价键,
属于离子化合物,
其中只有离子键的化合物的MgO、NaCl,MgO由Mg2+离子和O2-离子构成,MgO的电子式为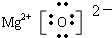 ;
;
NaCl由氯离子、钠离子构成,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,其电子式为 ;
;
故答案为:⑦⑩⑪⑫;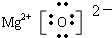 ;
; ;
;
(3)①②③⑤⑥⑧⑨,微粒间只存在共价键,其中二氧化硅是由Si和O以共价键结合在一起的原子晶体,其余都是含共价键的分子,①②③⑤⑥⑧⑨微粒间只存在共价键的化合物,所以属于共价化合物,
故答案为:①②③⑤⑥⑨;①②③⑤⑥⑧⑨.
点评 本题考查了化学键的判断,明确离子键和共价键的区别是解本题关键,注意离子化合物一定含有离子键,可能含有共价键,共价化合物只含共价键,只存在共价键的化合物不一定属于共价分子,可能属于原子晶体,为易错点,题目难度中等.

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案| 周期/族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,Na(用元素符号填写,下同)是最活泼的金属元素;F是最活泼的非金属元素.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)写出①的最高价氧化物的化学式CO2
(5)比较⑤与⑥的化学性质,Na更活泼.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③熔点:SO3>SiO2>CO2
④结合质子能力:OH->CH3COO->Cl-.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
| A. | Zn为负极,Ag2O是正极 | |
| B. | 在使用过程中,电池负极区溶液的c(OH-)值减小 | |
| C. | 电池工作时,电子由Zn极经外电路流向Ag2O极 | |
| D. | 电路中每通过0.2mol电子,负极的质量理论上减少6.5g |
| A. | CH2═CH-CH2CH2CH2CH3 | B. | CH3CH2CH═CHCH2CH3 | ||
| C. | CH3CH═CHCH2CH2CH3 | D. | 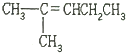 |
| A. | Na2C2O4水解:C2O42-+2H2O═H2C2O4+2OH- | |
| B. | NH4HSO3溶液与少量NaOH溶液混合:HSO3-+OH-═SO32-+H2O | |
| C. | 将FeS溶液加入过量稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| D. | 向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═CO32-+2HClO |
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | Na2O,NaOH,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物 |