题目内容
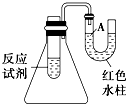 如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:
如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:(1)将铝片加入小试管内,然后注入足量稀盐酸,有关反应的离子方程式是
(2)U形导管中液面A
说明此反应是
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:(1)铝片与盐酸反应现象为铝片上有大量气泡生成,铝片不断溶解;
(2)铝片与盐酸的反应为放热反应,反应放出的热量使气体膨胀.
(2)铝片与盐酸的反应为放热反应,反应放出的热量使气体膨胀.
解答:
解:(1)铝片与盐酸反应的离子方程式为2Al+6H+═2Al3++3H2↑,反应现象为铝片上有大量气泡生成,铝片不断溶解,
故答案为:2Al+6H+═2Al3++3H2↑;铝片上有大量气泡生成,铝片逐渐溶解;
(2)铝片与盐酸的反应为放热反应,反应放出的热量使气体膨胀,使U形管液面A下降,
故答案为:下降;铝片与稀盐酸反应时放出热量,使锥形瓶内温度升高,气体压强增大;放热.
故答案为:2Al+6H+═2Al3++3H2↑;铝片上有大量气泡生成,铝片逐渐溶解;
(2)铝片与盐酸的反应为放热反应,反应放出的热量使气体膨胀,使U形管液面A下降,
故答案为:下降;铝片与稀盐酸反应时放出热量,使锥形瓶内温度升高,气体压强增大;放热.
点评:本题考查吸热反应和放热反应,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
在相同温度下,下列两个反应放出的热量分别用Q1和Q2表示:2H2(气)+O2(气)=2H2O(气)+Q1
2H2(气)+O2(气)=2H2O(液)+O2则Q1与O2的关系为( )
2H2(气)+O2(气)=2H2O(液)+O2则Q1与O2的关系为( )
| A、Q1<O2 |
| B、Q1>Q2 |
| C、Q1=Q2 |
| D、2Q1=Q2 |
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现,对两个反应的下列叙述中,错误的是( )
①Si (s)+3HCl(g)
SiHCl3(g)+H2(g)△H=-381kJ/mol
②SiHCl3(g)+H2(g)
Si (s)+3HCl(g)
①Si (s)+3HCl(g)
| ||
②SiHCl3(g)+H2(g)
| ||
| A、两个反应都是置换反应 |
| B、反应②是吸热反应 |
| C、两个反应互为可逆反应 |
| D、两个反应都是氧化还原反应 |
以下变化中需加氧化剂的是( )
| A、Cl-→Cl2 |
| B、Cu2+→Cu |
| C、CaCO3→CO2 |
| D、O2→Fe3O4 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下22.4LH2O中的分子数为NA |
| B、22.4LCl2所含分子数目为NA |
| C、23gNa变成Na+时失去的电子数目为NA |
| D、2g氢气所含原子数目为NA |
设NA为阿伏加德罗常数的值,下列叙述一定正确的是( )
| A、常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA |
| B、1mol羟基中的电子数为10NA |
| C、常温下,1molSiC中含有Si-C键的数目为4NA |
| D、28g铁粉与足量Cl2反应时转移的电子数为NA |
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B、分别加水稀释10倍,四种溶液的pH①>②>④>③ |
| C、①④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、VaL②与VbL③溶液混合后,若混合后溶液pH=7,则Va>Vb |