题目内容
设NA为阿伏加德罗常数的值,下列叙述一定正确的是( )
| A、常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA |
| B、1mol羟基中的电子数为10NA |
| C、常温下,1molSiC中含有Si-C键的数目为4NA |
| D、28g铁粉与足量Cl2反应时转移的电子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、溶液体积不明确;
B、根据羟基(-OH)不显电性来分析;
C、在SiC中每个Si与四个C相连;
D、铁与氯气反应后变为+3价.
B、根据羟基(-OH)不显电性来分析;
C、在SiC中每个Si与四个C相连;
D、铁与氯气反应后变为+3价.
解答:
解:A、由于溶液体积不明确,故无法计算液中氮原子数,故A错误;
B、羟基(-OH)不显电性,1mol羟基中含9mol电子,故B错误;
C、在SiC中每个Si与四个C相连,因此1mol SiC中含有Si-C键的物质的量为4mol,数目为4NA,故C正确;
D、28g铁粉的物质的量n=
=
=0.5mol,而铁与氯气反应后变为+3价,故0.5mol铁粉反应时转移1.5mol电子,个数为1.5NA,故D错误.
故选C.
B、羟基(-OH)不显电性,1mol羟基中含9mol电子,故B错误;
C、在SiC中每个Si与四个C相连,因此1mol SiC中含有Si-C键的物质的量为4mol,数目为4NA,故C正确;
D、28g铁粉的物质的量n=
| m |
| M |
| 28g |
| 56g/mol |
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
下列物质中属于电解质的是( )
| A、酒精 |
| B、NaHCO3 |
| C、CO2 |
| D、盐酸 |
已知:元素X、Y的核电荷数分别是a和b,它们的离子Xm+和Yn-的核外电子排布相同,则下列关系式中正确的是( )
| A、a-m=b+n |
| B、a+m=b-n |
| C、a-n=b+m |
| D、a+n=b-m |
2.84g X2O5中含0.1mol 氧原子,则X的相对原子质量是( )
| A、28.4 | B、31 |
| C、28 | D、14 |
下列表示对应化学反应的离子方程式正确的是( )
| A、用氨水溶解氢氧化铜沉淀:Cu2++4NH3?H2O=[Cu(NH3)4]2++4H2O |
| B、二氧化硫通入溴水溶液:SO2+Br2+2H2O=H2SO4+2Br-+2H+ |
| C、FeSO4酸性溶液中加入H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D、金属钠溶于水中:Na+H2O=Na++OH-+H2↑ |
下列说法正确的是( )
| A、硫酸和磷酸的摩尔质量相等 |
| B、2g氢气中含有1mol氢 |
| C、O2的摩尔质量(单位是g?mol-1)在数值上等于其相对分子质量 |
| D、1molCO的质量是28g?mol-1 |
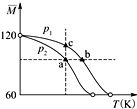 已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
已知(CH3COOH)2(g)?2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )| A、该过程的△H<0 |
| B、气体压强:p(a)<p(b)=p(c) |
| C、平衡常数:K(a)=K(b)<K(c) |
| D、测定乙酸的相对分子质量要在高压、低温条件 |
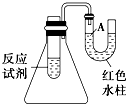 如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:
如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题: