题目内容
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现,对两个反应的下列叙述中,错误的是( )
①Si (s)+3HCl(g)
SiHCl3(g)+H2(g)△H=-381kJ/mol
②SiHCl3(g)+H2(g)
Si (s)+3HCl(g)
①Si (s)+3HCl(g)
| ||
②SiHCl3(g)+H2(g)
| ||
| A、两个反应都是置换反应 |
| B、反应②是吸热反应 |
| C、两个反应互为可逆反应 |
| D、两个反应都是氧化还原反应 |
考点:化学基本反应类型,氧化还原反应,吸热反应和放热反应
专题:物质的性质和变化专题
分析:A、置换反应是一种单质和一种化合物反应生成另一种单质和化合物的反应;
B、正向进行放热,则逆向进行吸热;
C、可逆反应是在同一条件下同时进行的反应;
D、反应过程中 元素化合价变化为氧化还原反应.
B、正向进行放热,则逆向进行吸热;
C、可逆反应是在同一条件下同时进行的反应;
D、反应过程中 元素化合价变化为氧化还原反应.
解答:
解:A、反应符合置换反应概念,故A正确;
B、反应①为放热反应,则其逆过程②为吸热反应,故B正确;
C、两个反应的反应条件不同,不能称为可逆反应,故C错误;
D、反应过程中元素化合价均有变化,所以都是氧化还原反应,故D正确;
故选C.
B、反应①为放热反应,则其逆过程②为吸热反应,故B正确;
C、两个反应的反应条件不同,不能称为可逆反应,故C错误;
D、反应过程中元素化合价均有变化,所以都是氧化还原反应,故D正确;
故选C.
点评:本题考查了反应类型判断,反应条件分析,注意可逆反应的分析判断,题目难度中等.

练习册系列答案
相关题目
下列关于丙烯(CH3-CH=CH2)的说法正确的( )
| A、丙烯分子中3个碳原子在同一直线上 |
| B、丙烯分子存在非极性键 |
| C、丙烯分子中3个碳原子都是sp3杂化 |
| D、丙烯分子有7个σ键,1个π键 |
在其他条件不变时,能使反应2SO2+2O2?2SO3速率加快的措施是( )
| A、升高温度 |
| B、减小生成物浓度 |
| C、增加反应物浓度 |
| D、减小压强 |
下列说法中正确的是( )
| A、元素性质随着相对原子质量的递增而呈周期性的变化叫元素周期律 |
| B、同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1、11或25 |
| C、在周期表中ⅠA族处寻找催化剂和耐高温的合金材料 |
| D、第三周期元素的离子半径,从左到右逐渐减小 |
下列性质可以证明氯化钠中一定存在离子键的是( )
| A、具有较高的熔点 |
| B、熔融状态能导电 |
| C、水溶液能导电 |
| D、常温下能溶于水 |
2.84g X2O5中含0.1mol 氧原子,则X的相对原子质量是( )
| A、28.4 | B、31 |
| C、28 | D、14 |
将0.1mol/L醋酸溶液加水稀释,下列说法正确的是( )
| A、溶液中c(H+)和c(OH-)都减小 |
| B、溶液中c(H+)增大 |
| C、醋酸电离平衡向右移动 |
| D、溶液的pH不变 |
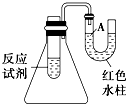 如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题:
如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题: