题目内容
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 44.Og14CO2与14N2O的混合物中所含中子数为22NA | |
| B. | 标准状况下,2.24L甲醛所含o键数目为0.3NA | |
| C. | 常温常压下,4.5gH2O与足量Na2O2反应转移的电子数目为0.5 NA | |
| D. | 50mL 18mol/L硫酸与足量Cu共热,转移的电子数为0.9NA |
分析 A、14CO2与14N2O的摩尔质量不同;
B、求出甲醛的物质的量,然后根据甲醛中含3条o键来分析;
C、求出水的物质的量,然后根据过氧化钠和水反应时,当有1mol水参与反应时,反应转移1mol电子来分析;
D、铜只能与浓硫酸反应,和稀硫酸不反应.
解答 解:A、14CO2与14N2O的摩尔质量不同,故44g混合物的物质的量无法计算,则含有的中子个数无法计算,故A错误;
B、标况下2.24L甲醛的物质的量为0.1mol,而甲醛中含3条o键,故0.1mol甲醛中含0.3NA条o键,故B正确;
C、4.5g水的物质的量为0.25mol,而过氧化钠和水反应时,当有1mol水参与反应时,反应转移1mol电子,故当有0.25mol水参与反应时,反应转移0.25NA个电子,故C错误;
D、铜只能与浓硫酸反应,和稀硫酸不反应,故浓硫酸不能反应完全,则转移的电子数小于0.9NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
11. 构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )
构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )
 构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )
构成原电池的条件有很多,其中一种就是利用电解质的浓度差构成“浓差电池”.当电解质中某离子的浓度越大时其氧化性或还原性越强.如图,甲池为3mol•L-1的AgNO3溶液,乙池为1mol•L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K2,断开K1,发现电流计指针发生偏转.下列说法不正确的是( )| A. | 一段时间后电流计指针将归零,此时可视为反应不再进行 | |
| B. | 当电流计指针归零后,闭合K1,断开K2后,乙池溶液浓度上升 | |
| C. | 当电流计指针归零后,闭合K1,断开K2后,乙中Ag电极质量增加 | |
| D. | 实验开始先闭合K2,断开K1,此时NO3-向B电极移动 |
12.以下有关有机物的应用或说法正确的是( )
| A. | 葡萄糖、蔗糖均可发生银镜反应 | |
| B. | 硫酸铵和乙酸铅均能使蛋白质发生变性 | |
| C. | 乙炔和乙醛均可合成聚合物 | |
| D. | 淀粉和油脂都是能发生水解反应的高分子化合物 |
7.下列实验操作或结论正确的是( )
| A. | 用CO2鉴别NaAlO2溶液和CH3COONa溶液 | |
| B. | 金属钠着火时,立即用泡沫灭火器进行灭火 | |
| C. | 浓硫酸溅到皮肤上时立即用大量水冲洗,再涂上NaHCO3溶液 | |
| D. | 向未知液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知液中一定存在SO42-或SO32- |
4.化学是一门以实验为基础的科学,化学实验是化学学习的重要内容.下列说法不正确的是( )
| A. | 从试剂瓶中取出的液体药品若有剩余,则不能再放回原试剂瓶 | |
| B. | 用稀盐酸洗涤盛放过石灰水的试剂瓶 | |
| C. | 蒸馏时蒸馏烧瓶中的液体不能超过蒸馏烧瓶的$\frac{2}{3}$ | |
| D. | 在天平的两托盘上各放一张质量相同的滤纸,将NaOH固体放在左盘滤纸上称量 |
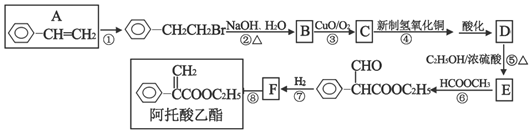
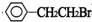 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$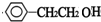 +NaBr.反应③的方程式
+NaBr.反应③的方程式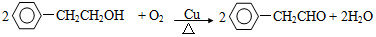 .
.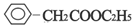 ;
;