题目内容
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下表:
溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中, 正确的是( )
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
A
【解析】
试题分析:A、向氯水中加入NaHCO3,碳酸氢钠与氢离子反应使氢离子浓度减小,Cl2+H2O H++Cl-+HClO平衡正向移动,次氯酸浓度增大,正确;B、四种溶液中,碱性最强的是碳酸钠,说明CO32-水解程度最大,盐的水解对水的电离起促进作用,所以水的电离程度最大的是碳酸钠,错误;C、根据盐溶液的pH判断NaHSO3的水解最弱,且亚硫酸氢根离子水解程度小于亚硫酸氢根离子的电离,所以相同物质的量浓度的H2SO3、H2CO3、HClO,亚硫酸的酸性最强,pH最小的是H2SO3,错误;D、NaHSO3溶液为酸性,亚硫酸氢根离子水解程度小于亚硫酸氢根离子的电离,c(Na+)> c(HSO3-) > c(H+)> c(SO32-)>c(OH-),错误,答案选A。
H++Cl-+HClO平衡正向移动,次氯酸浓度增大,正确;B、四种溶液中,碱性最强的是碳酸钠,说明CO32-水解程度最大,盐的水解对水的电离起促进作用,所以水的电离程度最大的是碳酸钠,错误;C、根据盐溶液的pH判断NaHSO3的水解最弱,且亚硫酸氢根离子水解程度小于亚硫酸氢根离子的电离,所以相同物质的量浓度的H2SO3、H2CO3、HClO,亚硫酸的酸性最强,pH最小的是H2SO3,错误;D、NaHSO3溶液为酸性,亚硫酸氢根离子水解程度小于亚硫酸氢根离子的电离,c(Na+)> c(HSO3-) > c(H+)> c(SO32-)>c(OH-),错误,答案选A。
考点:考查盐水解规律的应用,溶液中离子浓度的比较

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是 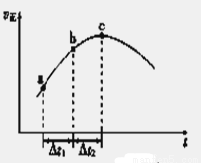
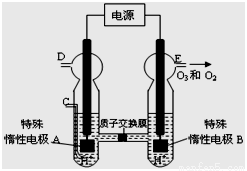
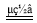 KIO3+3H2↑。下列有关说法不正确的是 ( )
KIO3+3H2↑。下列有关说法不正确的是 ( )