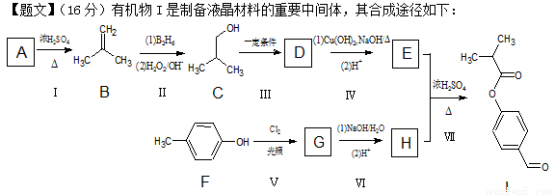
题目内容
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )

A.NH4Al(SO4)2 B.KAl(SO4)2
C.Al2(SO4)3 D.NaAlO2
C
【解析】
试题分析:加入氢氧化钡产生沉淀,后部分溶解,说明该化合物中一定 含有Al3+和SO42-离子,由图中的数据可知,最终得沉淀为3mol,说明硫酸根离子的物质的量是3mol,氢氧化铝与1mol氢氧化钡反应说明铝离子的物质的量是2mol,则需要3mol氢氧化钡生成氢氧化铝沉淀,符合此图,则溶液中Al3+和SO42-离子的物质的量之比是2:3,所以该物质是硫酸铝,答案选C。
考点:考查对物质成分的计算

练习册系列答案
相关题目
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下表:
溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中, 正确的是( )
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)

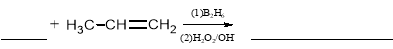 。
。 )的残留固体,若a点固体组成表示为PbOX或mPbO2·nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2·nPbO,列式计算x值和m:n值_ 。