题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA |
| B、1 L 0.1 mol.L-1的醋酸溶液中氢离子数为0.1 NA |
| C、以惰性电极电解NaCl溶液时,每放出11.2LCl2时,则消耗NaCl个数为NA |
| D、在密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移的电子数为0.6NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、S6与S8都是单质,则硫原子的物质的量为
=0.2mol;
B、醋酸为弱电解质,在水中发生部分电离;
C、惰性电极电解饱和NaCl溶液,阳极反应式2Cl--2e-=Cl2,11.2LCl2所处的状态不知,无法计算物质的量;
D、合成氨为可逆反应,不能进行到底.
| 6.4g |
| 32g/mol |
B、醋酸为弱电解质,在水中发生部分电离;
C、惰性电极电解饱和NaCl溶液,阳极反应式2Cl--2e-=Cl2,11.2LCl2所处的状态不知,无法计算物质的量;
D、合成氨为可逆反应,不能进行到底.
解答:
解:A、S6与S8都是单质,则硫原子的物质的量为
=0.2mol,则所含硫原子数一定为0.2NA,故A正确;
B、醋酸为弱电解质,在水中发生部分电离,因此溶液中氢离子数小于0.1 NA,故B错误;
C、惰性电极电解饱和NaCl溶液,阳极反应式2Cl--2e-=Cl2,11.2LCl2所处的状态不知,无法计算物质的量,故C错误;
D、合成氨为可逆反应,不能进行到底,因此转移电子书少于0.6NA,故D错误;
故选A.
| 6.4g |
| 32g/mol |
B、醋酸为弱电解质,在水中发生部分电离,因此溶液中氢离子数小于0.1 NA,故B错误;
C、惰性电极电解饱和NaCl溶液,阳极反应式2Cl--2e-=Cl2,11.2LCl2所处的状态不知,无法计算物质的量,故C错误;
D、合成氨为可逆反应,不能进行到底,因此转移电子书少于0.6NA,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的计算,为高考必考考点,综合性较强,注意混合物的组成、可逆反应的特征、气体摩尔体积的大小,难度一般.

练习册系列答案
相关题目
已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A、质子数:a>c>b>d |
| B、离子的还原性:Y2->Z- |
| C、离子半径:Y2->Z->X+>W3+ |
| D、元素电负性大小顺序:Y>Z |
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、27g铝的原子最外层电子总数为NA |
| B、2.8 g N2和2.8 g CO所含电子数均为1.4NA |
| C、1L0.1mol?L-1乙酸溶液中H+数为0.1NA |
| D、标准状况下,22.4L乙醇的分子数为NA |
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B、标准状况下,22.4L SO3的分子数为NA |
| C、1molFe在22.4L的Cl2(标准状况下)燃烧,转移的电子总数为3NA |
| D、电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |
某化合物6.4g在O2中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:2 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
测得VLAl2(SO4)3溶液中含Al3+mg,则该溶液中SO42-的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
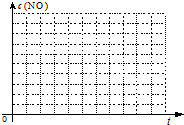
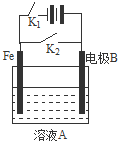 根据图示装置,下列说法不正确的是( )
根据图示装置,下列说法不正确的是( )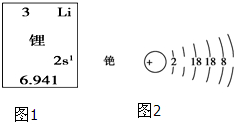 碱金属元素在科学研究与生产生活中有着非常广泛的用途.
碱金属元素在科学研究与生产生活中有着非常广泛的用途.